题目内容
6. 如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.(1)硫酸的摩尔质量为98g/mol
(2)该硫酸的物质的量浓度为18.4mol/L.
(3)现用该浓硫酸配制500mL 2mol/L的稀硫酸.需要用量筒量取上述浓硫酸
的体积为54.3mL(保留一位小数).
分析 (1)硫酸分子的相对分子质量为98,据此判断其摩尔质量;
(2)根据物质的量浓度c=$\frac{1000ρω}{M}$计算出该浓硫酸的物质的量浓度;
(3)配制过程中溶质硫酸的物质的量不变,据此计算出需要浓硫酸的体积.
解答 解:(1)硫酸的分子量为98,则硫酸的摩尔质量为98g/mol,
故答案为:98 g/mol;
(2)该浓硫酸物质的量浓度c=$\frac{1000ρω}{M}$=$\frac{1000×1.84×98%}{98}$mol/L=18.4mol/L,
故答案为:18.4;
(3)现用该浓硫酸配制500mL 2mol/L的稀硫酸,配制过程中硫酸的物质的量不变,则需要浓硫酸的体积为:V=$\frac{2mol/L×0.5L}{18.4mol/L}$≈0.0543L=54.3mL,
故答案为:54.3.
点评 本题考查了物质的量浓度的计算,他们难度中等,明确物质的量与摩尔质量、物质的量浓度的关系为解答关键,注意掌握物质的量浓度的概念及表达式,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.下列微粒和基团中,碳原子不满足最外层为8电子结构的是( )
| A. | 一氯甲烷(CH3Cl) | B. | 甲基(-CH3 ) | C. | 碳负离子(CH3-) | D. | 乙烯(C2H4) |
1.在一个2L的容器内充入6.0mol某气态反应物,经过3S后,它的浓度变成1.2mol/L,在3S内用该反应物浓度的变化表示的反应速率为( )
| A. | 0.6mol•L-1•S-1 | B. | 0.8mol•L-1•S-1 | C. | 0.4mol•L-1•S-1 | D. | 2.4mol•L-1•S-1 |
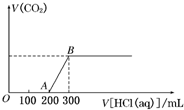 向100mL 3mol/L的NaOH溶液中缓慢通入一定量的CO2,充分反应得溶液X.在上述溶液X中,逐滴缓慢滴加1mol/L的盐酸,所得气体(不考虑溶解于水)的体积与所加盐酸的体积关系如图所示,求:
向100mL 3mol/L的NaOH溶液中缓慢通入一定量的CO2,充分反应得溶液X.在上述溶液X中,逐滴缓慢滴加1mol/L的盐酸,所得气体(不考虑溶解于水)的体积与所加盐酸的体积关系如图所示,求: