题目内容
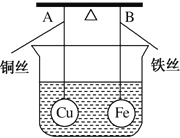
【题目】如图所示,杠杆AB两端分别挂有体积相同、质量相同的空心铜球和空心铁球,调节杠杆使其在水中保持平衡,然后小心地向烧杯中央滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中不考虑铁丝反应及两边浮力的变化)( )
A.杠杆为导体和绝缘体时,均为A端高B端低
B.杠杆为导体和绝缘体时,均为A端低B端高
C.当杠杆为绝缘体时,A端低B端高;为导体时,A端高B端低
D.当杠杆为绝缘体时,A端高B端低;为导体时,A端低B端高
【答案】D
【解析】
试题分析:杠杆为导体时,向烧杯中央滴入浓CuSO4溶液,构成Fe、Cu原电池,Fe为负极,发生Fe﹣2e﹣═Fe2+,Cu为正极,发生Cu2++2e﹣═Cu;
当杠杆为绝缘体时,只发生Fe与硫酸铜溶液的反应,以此来解答.
解:杠杆为导体时,向烧杯中央滴入浓CuSO4溶液,构成Fe、Cu原电池,Fe为负极,发生Fe﹣2e﹣═Fe2+,Cu为正极,发生Cu2++2e﹣═Cu,则A端低,B端高;
杠杆为绝缘体时,只发生Fe与硫酸铜溶液的反应,在Fe的表面附着Cu,质量变大,则A端高,B端低,
故选D.

练习册系列答案
 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目