题目内容
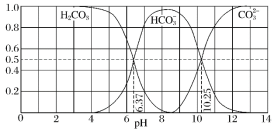
【题目】常温下含碳各微粒H2CO3、![]() 和
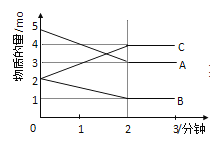
和![]() 存在于CO2和NaOH溶液反应后的溶液中,其物质的量分数与溶液pH的关系如图所示,下列说法错误的是( )
存在于CO2和NaOH溶液反应后的溶液中,其物质的量分数与溶液pH的关系如图所示,下列说法错误的是( )
A.pH=10.25时,c(Na+)=c(![]() )+c(
)+c(![]() )
)
B.为获得尽可能纯的NaHCO3,宜控制溶液的pH为7~9之间
C.根据图中数据,可以计算得到H2CO3第一步电离的平衡常数K1(H2CO3)=10-6.37
D.若是0.1molNaOH反应后所得的1L溶液,pH=10时,溶液中存在以下关系:c(Na+)>c(![]() )>c(
)>c(![]() )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
【答案】A
【解析】
A.pH=10.25时,溶质为碳酸钠和碳酸氢钠,碳酸钠溶液中满足物料守恒:![]() ,碳酸氢钠溶液中存在物料守恒:
,碳酸氢钠溶液中存在物料守恒:![]() ,则混合液中
,则混合液中![]() ,故A说法错误;
,故A说法错误;
B.根据图示可知,pH在79之间,溶液中主要存在![]() ,该pH范围内可获得较纯的NaHCO3,故B说法正确;
,该pH范围内可获得较纯的NaHCO3,故B说法正确;
C.根据图象曲线可知,pH=6.37时,H2CO3和![]() 的浓度相等,碳酸的第一步电离的平衡常数
的浓度相等,碳酸的第一步电离的平衡常数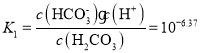 ,故C说法正确;
,故C说法正确;
D.pH=10时的溶液为碱性,则c(OH)>c(H+),溶质为碳酸钠和碳酸氢钠,c(Na+)离子浓度最大,结合图象曲线变化可知:![]() ,OH-为
,OH-为![]() 、
、![]() 水解所得,水解程度微弱,因此离子浓度大小为:
水解所得,水解程度微弱,因此离子浓度大小为:![]() ,故D说法正确;
,故D说法正确;
综上所述,说法错误的是A,故答案为:A。

【题目】298 K时,![]() γ-羟基丁酸水溶液发生如下反应,生成
γ-羟基丁酸水溶液发生如下反应,生成![]() 丁内酯: HOCH2CH2CH2COOH
丁内酯: HOCH2CH2CH2COOH![]()
![]() +H2O
+H2O
不同时刻测得![]() 丁内酯的浓度如下表。
丁内酯的浓度如下表。
| 20 | 50 | 80 | 100 | 120 | 160 | 220 | ∞ |
| 0.024 | 0.050 | 0.071 | 0.081 | 0.090 | 0.104 | 0.116 | 0.132 |
注:该条件下副反应、溶液体积变化忽略不计。下列分析正确的是
A.增大γ-羟基丁酸的浓度可提高γ-丁内酯的产率
B.298 K时,该反应的平衡常数为2.75
C.反应至120 min时,γ-羟基丁酸的转化率<50%
D.80~120 min的平均反应速率:v(γ-丁内酯) >1.2×10-3 mol L-1min-1
【题目】二甲醚又称甲醚,简称DME,熔点-141.5 ℃,沸点-24.9 ℃,与石油液化气(LPG)相似,被誉为“21世纪的清洁燃料”。制备原理如下:
Ⅰ.由天然气催化制备二甲醚:
①2CH4(g)+O2(g) =CH3OCH3(g)+H2O(g) ΔH1
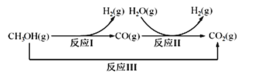
Ⅱ.由合成气制备二甲醚:
②CO(g)+2H2(g) ![]() CH3OH(g) ΔH2=-90.7 kJ·mol-1
CH3OH(g) ΔH2=-90.7 kJ·mol-1
③2CH3OH(g) ![]() CH3OCH3(g)+H2O(g) ΔH3
CH3OCH3(g)+H2O(g) ΔH3
回答下列问题:
(1)若甲烷和二甲醚的燃烧热分别是890.3 kJ·mol-1、1 453.0 kJ·mol-1;1 mol液态水变为气态水要吸收44.0 kJ的热量。反应③中的相关的化学键键能数据如表:
化学键 | H-H | C-O | H-O(水) | H-O(醇) | C-H |
E (kJ · mol-1) | 436 | 343 | 465 | 453 | 413 |
则ΔH1=______kJ·mol-1;ΔH3=______ kJ·mol-1
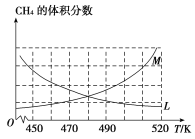
(2)反应③的化学平衡常数表达式为______________。制备原理Ⅰ中,在恒温、恒容的密闭容器中合成,将气体按n(CH4)∶n(O2)=2∶1混合,能正确反映反应①中CH4 的体积分数随温度变化的曲线是_________________。下列能表明反应①达到化学平衡状态的是_______________。
A.混合气体的密度不变
B.反应容器中二甲醚的百分含量不变
C.反应物的反应速率与生成物的反应速率之比等于化学计量数之比
D.混合气体的压强不变
(3)有人模拟制备原理Ⅱ,在500 K时的2 L的密闭容器中充入2 mol CO和6 mol H2,8 min达到平衡,平衡时CO的转化率为80%,c(CH3OCH3)=0.3 mol·L-1,用H2表示反应②的速率是__________;可逆反应③的平衡常数K3=_________。若在500 K时,测得容器中n(CH3OH)=n(CH3OCH3),此时反应③v(正)_________v(逆),说明原因____________________。