题目内容
下列反应的离子方程式正确的是( )
| A、将氢碘酸加到Fe(OH)3胶体中:Fe(OH)3+3H+═Fe3++3H2O |
| B、碳酸氢钙溶液中中入少量烧碱:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+H2O |
| C、新制氯水中滴入少量溴化亚铁溶液:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- |
| D、锌与1mol/L-1 HNO3溶液反应:Zn+2H+═Zn2++H2↑ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.发生氧化还原反应生成碘化亚铁、碘、水;
B.反应生成碳酸钙、水、碳酸氢钠;
C.少量溴化亚铁完全被氧化;
D.发生氧化还原反应生成硝酸锌、NO和水.
B.反应生成碳酸钙、水、碳酸氢钠;
C.少量溴化亚铁完全被氧化;
D.发生氧化还原反应生成硝酸锌、NO和水.
解答:
解:A.将氢碘酸加到Fe(OH)3胶体中的离子反应为2Fe(OH)3+2I-+6H+═2Fe2++I2+6H2O,故A错误;
B.碳酸氢钙溶液中中入少量烧碱的离子反应为Ca2++HCO3-+OH-═CaCO3↓+H2O,故B错误;
C.新制氯水中滴入少量溴化亚铁溶液的离子反应为2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl-,故C正确;
D.锌与1mol/L-1 HNO3溶液反应的离子反应为3Zn+2NO3-+8H+═3Zn2++2NO↑+4H2O,故D错误;
故选C.
B.碳酸氢钙溶液中中入少量烧碱的离子反应为Ca2++HCO3-+OH-═CaCO3↓+H2O,故B错误;
C.新制氯水中滴入少量溴化亚铁溶液的离子反应为2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl-,故C正确;
D.锌与1mol/L-1 HNO3溶液反应的离子反应为3Zn+2NO3-+8H+═3Zn2++2NO↑+4H2O,故D错误;
故选C.
点评:本题考查离子反应的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应及与量有关的离子反应考查,题目难度不大.

练习册系列答案
 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案
相关题目
能证明SO2具有漂白性的实验是( )
| A、SO2使酸性KMnO4溶液褪色 |
| B、SO2使溴水褪色 |
| C、SO2使品红溶液褪色 |
| D、SO2使含酚酞的NaOH溶液褪色 |
下列叙述与对应图式正确的是( )
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径 | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 主要化合价 | -2 | +2 | +1 | +5、-3 | +7、-1 | +1 | +5、-3 | +3 |
| A、由下列短周期元素性质的数据推断元素③最高价氧化物对应的水化物碱性最强 |
B、 如图装置中,待镀铁制品应与电源负极相连 |
C、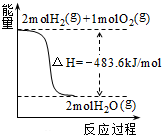 如图表示H2与O2发生反应过程中的能量变化,则H2的燃烧热的热化学方程式为:2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ/mol |
D、 如图表示某一放热反应,若使用催化剂E1、E2、△H都会发生改变 |
下列物质中,加入10mL HCl溶液时,其pH不会改变的是( )
| A、20mL同一浓度的HCl溶液 |
| B、20mL NH4Cl溶液 |
| C、10mL水 |
| D、10mL稀NaOH溶液 |
某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2,已知该反应中H2O2只发生如下过程:H2O2→O2.则下列说法中正确的是( )
| A、上述过程的氧化剂为H2O2 | ||
B、若上述过程中产生的氧气为1mol,则消耗的H2CrO4为
| ||
| C、上述过程中Cr(OH)3是反应物 | ||
| D、上述过程的氧化产物为H2CrO4 |
c(H+)相等的盐酸和醋酸溶液都稀释相同的倍数后,pH的大小关系是( )
| A、盐酸>醋酸 | B、醋酸>盐酸 |
| C、盐酸=醋酸 | D、无法判断 |
化学与生活密切相关,下列说法不正确的是( )
| A、葡萄糖可用于补钙药物的合成 |
| B、二氧化硫可广泛用于食品的漂白 |
| C、聚乙烯塑料制品可用于食品的包装 |
| D、次氯酸钠溶液可用于环境的消毒杀菌 |