题目内容
【题目】甲乙两容器中发生相同的反应:A(g)+3B(g)![]() 2C(g),甲恒容、乙恒压,温度相同而恒定。起始时甲中加入0.01mol A和0.03mol B,乙中加入0.02mol C,开始时两容器压强相等,最后分别达到平衡。下列有关它们平衡状态的叙述正确的是( )
2C(g),甲恒容、乙恒压,温度相同而恒定。起始时甲中加入0.01mol A和0.03mol B,乙中加入0.02mol C,开始时两容器压强相等,最后分别达到平衡。下列有关它们平衡状态的叙述正确的是( )
A.体积:甲可能小于乙B.C的物质的量:甲一定小于乙
C.压强:甲可能大于乙D.A、C浓度比值![]() :甲一定小于乙
:甲一定小于乙
【答案】B
【解析】
在甲、乙两容器中分别发生反应A(g)+3B(g)![]() 2C(g),甲恒容、乙恒压,温度相同且恒定,起始时甲中加入0.01mol A和0.03mol B,乙中加入0.02mol C气体,开始时两容器压强相等,最后分别达到平衡,根据等效平衡理论进行问题的分析。
2C(g),甲恒容、乙恒压,温度相同且恒定,起始时甲中加入0.01mol A和0.03mol B,乙中加入0.02mol C气体,开始时两容器压强相等,最后分别达到平衡,根据等效平衡理论进行问题的分析。
在甲、乙两容器中分别发生反应A(g)+3B(g)![]() 2C(g),甲恒容、乙恒压,温度相同且恒定,起始时甲中加入0.01mol A和0.03mol B,乙中加入0.02mol C气体,开始时两容器压强相等,最后分别达到平衡;
2C(g),甲恒容、乙恒压,温度相同且恒定,起始时甲中加入0.01mol A和0.03mol B,乙中加入0.02mol C气体,开始时两容器压强相等,最后分别达到平衡;
A、反应是气体体积减小的反应,甲恒容体积不变,乙恒压体积减小,所以体积甲不可能小于乙,A错误;
B、反应是气体体积减小的反应,甲恒容体积不变,反应后压强减小,乙恒压,所以乙比甲平衡后进行程度大,则平衡时乙中C的物质的量大,故C的物质的量:甲一定小于乙,B正确;
C.反应是气体体积减小的反应,甲恒容压强减小,乙恒压压强不变,所以压强:甲不可能大于乙,C错误;
D.反应是气体体积减小的反应,甲恒容压强减小,乙恒压压强不变,所以乙比甲平衡后进行程度大,平衡时乙中C的物质的量大,则浓度比![]() :甲一定大于乙,D错误;
:甲一定大于乙,D错误;
故选B。

 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案【题目】根据下列实验能得出相应结论的是
选项 | 实验 | 结论 |
A | 常温下,测得0.1mol/LNaA溶液的pH小于0.1mol/L Na2CO3溶液的pH | 酸性:HA>H2CO3 |
B | 向含有淀粉的FeI2溶液中加入足量溴水,溶液变蓝色 | 还原性:I->Fe2+ |
C | 向饱和FeSO4溶液中加入CuS固体,测得溶液中c(Fe2+)不变 | Ksp(CuS)<Ksp(FeS) |
D | 向氨水中滴加少量AgNO3溶液,无沉淀生成 | Ag+与NH3·H2O能大量共存 |
A. A B. B C. C D. D
【题目】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
(1)如图是N2(g)和H2(g)反应生成1 mol NH3(g)过程中能量的变化示意图,请写出N2和H2反应的热化学方程式:_______。
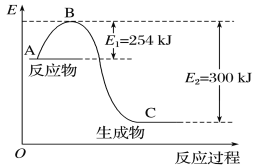
(2)若已知下列数据:
化学键 | H—H | N≡N |
键能/kJ·mol-1 | 435 | 943 |
试根据表中及图中数据计算N—H的键能:___kJ·mol-1。
(3)捕碳技术(主要指捕获CO2在降低温室气体排放中具有重要的作用。目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下反应:
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)=(NH4)2CO3(aq) ΔH1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g)=NH4HCO3(aq) ΔH2
反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g)=2NH4HCO3(aq) ΔH3
请回答下列问题:
ΔH3与ΔH1、ΔH2之间的关系是ΔH3=___。
(4)试比较下列两组△H的大小(填“>”、“<”或“=”)
①H2(g)+![]() O2(g)=H2O(g) △H1 H2(g)+
O2(g)=H2O(g) △H1 H2(g)+![]() O2(g)=H2O(l) △H2
O2(g)=H2O(l) △H2
则△H1____△H2
②S(s)+O2(g)=SO2(g) △H3
Ba(OH)2·8H2O(s)+2NH4Cl(s)=BaCl2(s)+10H2O(l)+2NH3(g) △H4
则△H3______△H4