题目内容
【题目】下列说法正确的是( )
A.标准状况下,22.4LHF中含有的氟原子数目为NA(NA表示阿伏加德罗常数)
B.0.1 mol/L的NH4HSO4溶液中滴加0.1 mol/L的Ba(OH)2溶液至沉淀刚好完全:c(NH4+)>c(OH-)>c(SO42-)>c(H+)
C.1mol如图所示 物质与浓溴水反应时通常最多消耗Br2为4mol
物质与浓溴水反应时通常最多消耗Br2为4mol
D.常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H>0,一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率
【答案】C
【解析】
A. 标准状况下HF为液体,不能使用气体摩尔体积计算,A错误;
B. 0.1 mol/L的NH4HSO4溶液中滴加0.1 mol/L的Ba(OH)2溶液至沉淀刚好完全,二者恰好反应生成一水合氨、水和硫酸钡沉淀,所以溶液中的溶质是一水合氨,还有BaSO4沉淀,溶液中的离子浓度为:c(OH-)>c(NH4+)>c(H+)>c(SO42-),B错误;
C.苯环上酚羟基的邻对位氢原子能被溴原子取代,溴能和碳碳双键发生加成反应,所以1 mol该物质与浓溴水反应时最多消耗Br2为4 mol,C正确;
D.常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,△G=△H-T△S,△S>0,△G>0,故该反应△H>0,催化剂只能改变化学反应的速率,对化学平衡不产生影响,D错误;
故合理选项是C。

 名题金卷系列答案
名题金卷系列答案【题目】第四周期的Cr、Fe、Co、Ni、Cu、Zn等许多金属能形成配合物,单质铁、砷及它们的化合物广泛应用于超导体材料等领域,请回答下列问题:
(1)Fe2+的核外电子排布式为_________________。
(2)NH3是一种很好的配体,NH3的沸点______(填“>”“=”或“<”)AsH3。
(3)N原子核外有______种不同运动状态的电子。基态N原子中,能量最高的电子所占据的原子轨道的形状为_____。
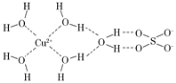
(4)科学家通过X射线测得胆矾结构示意图可简单表示如图,图中虚线表示的作用力为________。
(5)As的卤化物的熔点如下:
AsCl3 | AsBr3 | AsI3 | |
熔点/K | 256.8 | 304 | 413 |
表中卤化物熔点差异的原因是________________。
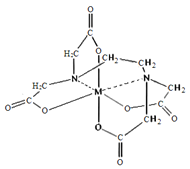
(6)向FeCl3溶液中滴入EDTA试剂可得配合物A,其结构如图所示,图中M代表Fe3+,则Fe3+与氮原子之间形成的化学键是_______,Fe3+的配位数为______。