题目内容
【题目】按如图所示的装置和以下实验步骤,可以制取少量的溴苯和溴乙烷.已知乙醇在一定条件下与氢溴酸反应可制备溴乙烷:
C2H5OH+HBr→C2H5Br+H2O
主要实验步骤如下:①连接好装置,检查装置的气密性;②向烧瓶中加入一定量的苯和液溴.向锥形瓶中加入乙醇和浓H2SO4的混合液至稍高于进气导管口处;③将A装置中的纯铁丝小心向下插入混合液中;④点燃B装置中的酒精灯,用小火缓缓对锥形瓶加热10min.
请填写下列空白:
(1)写出制取溴苯的化学方程式: .
(2)步骤③中观察到的现象是: .
(3)C装置中U形管内部用蒸馏水封住管底的作用是: .
(4)反应完毕后,U形管内的现象是: . 分离溴乙烷时所用的最主要仪器的名称是(只填一种) .
(5)实验结束,从烧瓶的混合物中分离出粗制黄色的溴苯,产生黄色的原因是其中含有(填化学式).欲得到无色的溴苯的方法是(填试剂和操作名称).
【答案】
(1)C6H6+Br2 ![]() C6H5Br+HBr
C6H5Br+HBr
(2)剧烈反应,瓶上方有红棕色气体产生
(3)一是溶解溴化氢、二是液封(防止产物及溴化氢挥发)
(4)U形管中蒸馏水底部有无色油状液体;分液漏斗
(5)Br2;用NaOH溶液洗涤分液
【解析】解:(1)将A装置中的纯铁丝小心向下插入混合液中,铁和溴反应生成三溴化铁,2Fe+3Br2=2FeBr3 , 三溴化铁与苯作用,生成溴苯和铁,同时有溴化氢生成,铁作催化剂,所以制备溴苯的化学反应方程式为:C6H6+Br2 ![]() C6H5Br+HBr, 所以答案是:C6H6+Br2
C6H5Br+HBr, 所以答案是:C6H6+Br2 ![]() C6H5Br+HBr;(2)苯和液溴在铁粉催化作用下发生取代反应生成溴苯和溴化氫,该反应为放热反应且反应剧烈,苯和溴单质沸点低,易挥发,溴蒸气为红棕色,所以步骤③中观察到的现象是:剧烈反应,瓶上方有红棕色气体产生,
C6H5Br+HBr;(2)苯和液溴在铁粉催化作用下发生取代反应生成溴苯和溴化氫,该反应为放热反应且反应剧烈,苯和溴单质沸点低,易挥发,溴蒸气为红棕色,所以步骤③中观察到的现象是:剧烈反应,瓶上方有红棕色气体产生,
所以答案是:剧烈反应,瓶上方有红棕色气体产生;(3)CH3CH2Br难溶于水,溴化氢极易溶于水,形成的氢溴酸是强酸,U形管内的蒸馏水用来溶解吸收HBr,防止HBr及CH3CH2Br逸出,
所以答案是:一是溶解溴化氢、二是液封(防止产物及溴化氢挥发);(4)溴乙烷是一种无色的油状液体物质,和水是互不相溶的,反应完毕,U形管内会发生液体分层现象,上层为水层,下层为无色油状液体(溴乙烷),可以采用分液的方法来实现物质的分离,最主要仪器为分液漏斗,
所以答案是:U形管中蒸馏水底部有无色油状液体;分液漏斗;(5)过量的溴溶解在溴苯中而使溴苯显黄色,常温下,氢氧化钠可以和溴单质反应,和溴苯不互溶,不反应,欲得到无色的溴苯可用NaOH溶液洗涤:2NaOH+Br2═NaBr+NaBrO+H2O,再用分液的方法分离,
所以答案是:Br2;用NaOH溶液洗涤分液.

【题目】碳酸钙、盐酸是中学化学实验中的常用试剂.
(1)甲同学拟测定CaCO3固体与过量0.1molL﹣1 HCl的反应速率.
①该反应的离子方程式为 .
②设计实验方案:通过测量计算反应速率
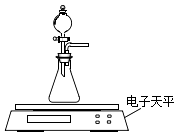
(2)乙同学拟用如图装置探究固体表面积和反应物浓度对化学反应速率的影响.电子天平限选试剂与用品:0.1molL﹣1 HCl、颗粒状CaCO3、粉末状CaCO3、蒸馏水、量筒、秒表
(i)设计实验方案:在反应物浓度或固体表面积不同的条件下,测定
(要求所测得的数据能直接体现反应速率大小).
(ⅱ) 根据(i)中设计的实验测定方案,拟定实验表格,完整体现实验方案.列出所用试剂的用量、待测物理量;数据用字母a、b、c、d表示.
已知实验1和2探究固体表面积对反应速率的影响;
实验1和3探究反应物浓度对反应速率的影响.
写出表中①﹣⑥所代表的必要数据或物理量
物理量 | V(0.1molL﹣1 HCl)/mL | m(颗粒状CaCO3)/g | m(粉末状CaCO3)/g | V(蒸馏水)/mL | ⑤ | ⑥ |
实验1 | a | b | 0 | c | d | |
实验2 | 0 | c | d | |||
实验3 | c | 0 | d |