��Ŀ����
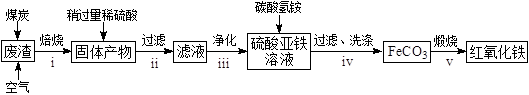
����Ŀ������һ�����ȼ������ۺ���������ĩ�Ļ����ڸ�����ʹ֮��ַ�Ӧ������Ӧ��Ĺ����Ϊ���ȷݣ���������ʵ�飨����Ũ��ʱ�ٶ���Һ���û�б仯����
��������һ�ݹ����м���100mL 2.0mol/L��NaOH��Һ������ʹ���ַ�Ӧ����ˣ������Һ��c��OH-����1mol/L��
������һ�ݹ����м���140mL 4��0 mol/L��HCl��Һ��ʹ����ȫ���ܽ⣬��÷�Ӧ��������Һ��ֻ��H+��Fe2+��Al3+������������c��H+��=1mol/L��
��1��д�������ȷ�Ӧ�Ļ�ѧ����ʽ��_______________________________
д��ʵ��ٷ��������ӷ���ʽ��_________________________________��
��2��������ȼ������۵�����Ϊ___________________________��
��3��������ȼ�����������ĩ������Ϊ__________________________________��
���𰸡� 2Al+Fe2O3![]() 2Fe+Al2O3 Al2O3+2OH-=AlO2-+2H2O��2Al+2H2O+2OH-=2AlO2-+3H2�� 5.4g 9.6g
2Fe+Al2O3 Al2O3+2OH-=AlO2-+2H2O��2Al+2H2O+2OH-=2AlO2-+3H2�� 5.4g 9.6g
����������1�����ȷ�Ӧ�������������ڸ��������·�Ӧ������������������Ӧ�Ļ�ѧ����ʽΪ��2Al+Fe2O3![]() 2Fe+Al2O3��ʵ������ȷ�Ӧ��Ļ�����������������ã�����ֻ����������δ��Ӧ�������������Ʒ�Ӧ�����������ӷ���ʽ�У�Al2O3+2OH-=AlO2-+2H2O��2Al+2H2O+2OH-=2AlO2-+3H2����ʵ�������ȥn(NaOH)��100mL��(2.0mol/L��1.0mol/L)��0.1mol��������Al����Al2O3����NaOH��Һ��Ӧ������NaAlO2�����ȼ�����n(Al)��n(NaOH)��2��0.2mol��m(Al)��5.4g��ʵ���������Һ�У����ݡ�����غ㡱��n(H+)��2��n(Fe2+)��3��n(Al3+)��n(Cl��)����n(Fe2+)��
2Fe+Al2O3��ʵ������ȷ�Ӧ��Ļ�����������������ã�����ֻ����������δ��Ӧ�������������Ʒ�Ӧ�����������ӷ���ʽ�У�Al2O3+2OH-=AlO2-+2H2O��2Al+2H2O+2OH-=2AlO2-+3H2����ʵ�������ȥn(NaOH)��100mL��(2.0mol/L��1.0mol/L)��0.1mol��������Al����Al2O3����NaOH��Һ��Ӧ������NaAlO2�����ȼ�����n(Al)��n(NaOH)��2��0.2mol��m(Al)��5.4g��ʵ���������Һ�У����ݡ�����غ㡱��n(H+)��2��n(Fe2+)��3��n(Al3+)��n(Cl��)����n(Fe2+)��![]() ��0.06mol�����ȼ���n(Fe2O3)��n(Fe2+)��
��0.06mol�����ȼ���n(Fe2O3)��n(Fe2+)��![]() ��2��0.06mol��m(Fe2O3)��9.6g��
��2��0.06mol��m(Fe2O3)��9.6g��