题目内容
6.阿伏加德罗常数约为6.02×1023mol-1,下列说法正确的是( )| A. | 标准状况下22.4 L NO与11.2 L O2混合后所得气体分子数为6.02×1023 | |
| B. | 标准状况下3.36 L CCl4含碳原子数为0.15×6.02×1023 | |
| C. | 1 mol甲基(-CH3)中所含电子数为9×6.02×1023 | |
| D. | 2 L 1 mol•L-1 的盐酸中所含氯化氢分子数为2×6.02×1023 |
分析 A、NO2气体中存在平衡:2NO2?N2O4;
B、标况下,四氯化碳为液态;
C、甲基不显电性;
D、盐酸溶液中无HCl分子.
解答 解:A、标准状况下22.4 L NO即1molNO与11.2 L O2即0.5mol氧气反应生成1molNO2,而NO2气体中存在平衡:2NO2?N2O4,使分子个数减小,所得气体分子数小于6.02×1023,故A错误;
B、标况下,四氯化碳为液态,故不能根据气体摩尔体积来计算,故B错误;
C、甲基不显电性,1mol甲基含9mol电子,即9×6.02×1023个,故C正确;
D、HCl溶于水后完全电离,故盐酸溶液中无HCl分子,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目
16.某单烯烃与氢气的加成产物为:(CH3 )2CHCH2CH3,下列相关说法正确的是( )
| A. | 该产物的名称是1,1-二甲基丙烷 | |
| B. | 1mol加成产物燃烧消耗6.5mol氧气 | |
| C. | 原单烯烃只可能有3种不同结构 | |
| D. | 原烯烃与分子式是C3H6的烃一定互为同系物 |
17.同主族元素所形成的同一类型的化合物结构和性质往往相似,已知化合物PH4I是一种无色晶体,试判断下列对其描述正确的是( )
| A. | PH4I加热易分解,且可产生紫红色气体 | |
| B. | PH4I很稳定,加热不易分解 | |
| C. | PH4I不能与NaOH反应 | |
| D. | PH4I不能由PH3与HI化合生成 |
14.恒容密闭容器中的可逆反应H2(g)+I2(g)?2HI(g),达到反应限度时的标志是( )
| A. | 混合气体的密度恒定不变 | B. | 混合气体的颜色不再改变 | ||
| C. | H2、I2、HI的浓度相等 | D. | 气体总物质的量不变 |
1. 某温度下,向一定体积0.1mol/LNaOH溶液中逐滴加入等浓度的CH3COOH溶液,溶液中pOH[pOH=-lgc(OH-)]与pH的变化关系如图所示,则下列说法错误的是( )
某温度下,向一定体积0.1mol/LNaOH溶液中逐滴加入等浓度的CH3COOH溶液,溶液中pOH[pOH=-lgc(OH-)]与pH的变化关系如图所示,则下列说法错误的是( )
 某温度下,向一定体积0.1mol/LNaOH溶液中逐滴加入等浓度的CH3COOH溶液,溶液中pOH[pOH=-lgc(OH-)]与pH的变化关系如图所示,则下列说法错误的是( )
某温度下,向一定体积0.1mol/LNaOH溶液中逐滴加入等浓度的CH3COOH溶液,溶液中pOH[pOH=-lgc(OH-)]与pH的变化关系如图所示,则下列说法错误的是( )| A. | Q点消耗CH3COOH溶液的体积等于NaOH溶液的体积 | |
| B. | M、Q、N三点都满足:C(Na+)+C(H+)═c(CH3COO-)+C(OH-) | |
| C. | M点和N点所示溶液中水的电离程度相同 | |
| D. | N点所示溶液中c(CH3COO-)<c(Na+) |
11.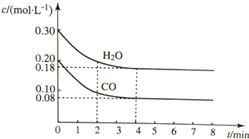 在容积为10L的容器中,通入一定量的CO和H2O(g),在850℃时发生反应CO(g)+H2O?CO2(g)+H2(g)△H<0.CO和H2O浓度变化如图所示.
在容积为10L的容器中,通入一定量的CO和H2O(g),在850℃时发生反应CO(g)+H2O?CO2(g)+H2(g)△H<0.CO和H2O浓度变化如图所示.
(1)则0~4min内反应速率v(CO)为0.03mol/(L•min);
(2)1000℃时,在相同容器中发生上述反应,容器内各物质的浓度变化如下表.
1000℃时物质浓度的变化
①c1数值>0.08mol/L(填“<”“>”或“=”);
②表中5~6min之间数值发生变化,可能的原因是a(填字母).
a.增加水蒸气
b.降低温度
c.使用催化剂
d.增加氢气浓度.
 在容积为10L的容器中,通入一定量的CO和H2O(g),在850℃时发生反应CO(g)+H2O?CO2(g)+H2(g)△H<0.CO和H2O浓度变化如图所示.
在容积为10L的容器中,通入一定量的CO和H2O(g),在850℃时发生反应CO(g)+H2O?CO2(g)+H2(g)△H<0.CO和H2O浓度变化如图所示.(1)则0~4min内反应速率v(CO)为0.03mol/(L•min);
(2)1000℃时,在相同容器中发生上述反应,容器内各物质的浓度变化如下表.
1000℃时物质浓度的变化
| t/min | c(CO)/(mol•L-1) | c(H2O)/(mol•L-1) | c(CO2)/(mol•L-1) | c(H2)/(mol•L-1) |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 1 | 0.138 | 0.238 | 0.062 | 0.062 |
| 2 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | 0.084 |
| 6 | 0.096 | 0.266 | 0.104 | 0.104 |
②表中5~6min之间数值发生变化,可能的原因是a(填字母).
a.增加水蒸气
b.降低温度
c.使用催化剂
d.增加氢气浓度.
 硫酸亚铁晶体(FeSO4•7H2O)在医药上作补血剂.某课外小组的同学欲测定该补血剂中铁元素的含量.实验步骤如图:
硫酸亚铁晶体(FeSO4•7H2O)在医药上作补血剂.某课外小组的同学欲测定该补血剂中铁元素的含量.实验步骤如图: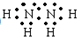 ,过氧化氢的结构式:
,过氧化氢的结构式: .
.

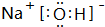 ; 用电子式表示G与Q形成化合物的过程
; 用电子式表示G与Q形成化合物的过程 ;
;