题目内容
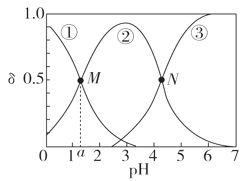
【题目】某温度下,弱酸H2A溶液中,存在H2A、HA-和A2-三种形态的粒子,其物质的量分数δ[δ(X)=![]() ]随溶液pH变化的关系如图所示,下列说法错误的是
]随溶液pH变化的关系如图所示,下列说法错误的是
A.pH>4的溶液中,δ(A2-)=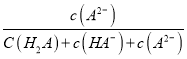 ,
,
B.M点对应的溶液中水的电离程度小于N点
C.若图中a为1.2,则lg [Ka1(H2A)]=-1.2
D.曲线②代表的粒子是HA-
【答案】A
【解析】
随着溶液的pH增大,溶液中c (H2A) 减小、c (HA-)先增大后减小、c (A2-)增大,所以①为c (H2A) 物质的量分数,②为c (HA-)物质的量分数,③为c (A2-)物质的量分数,据此解答本题。
当pH>4后,由图像可知,溶液中几乎没有H2A,此时,δ(A2-)=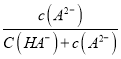 ,故A错误;
,故A错误;
B、随着溶液pH增大,酸对水的电离抑制作用减小,所以N点对应的溶液中水的电离程度大于M点,故B正确;
C、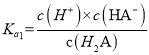 ,由图像可知,此时δ(H2A)=0.5,即c(H2A)= c(HA-),所以Ka1=10-1.2,所以lg [Ka1(H2A)]=-1.2,故C正确;
,由图像可知,此时δ(H2A)=0.5,即c(H2A)= c(HA-),所以Ka1=10-1.2,所以lg [Ka1(H2A)]=-1.2,故C正确;
D、由分析可知,曲线②代表的粒子是HA-故D正确;
故选A。

练习册系列答案
相关题目
【题目】从下列实验事实或操作所引出的相应结论正确的是( )
选项 | 实验事实或操作 | 结论 |
A | 其他条件相同, | 当其他条件不变时,增大反应物浓度化学反应速率加快 |
B | 在化学反应前后,催化剂的质量和化学性质都没有发生改变 | 催化剂一定不参与化学反应 |
C | 物质的量浓度相同的盐酸和醋酸分别与等质量的形状相同的锌粒反应 | 开始时的反应速率相同 |
D | 在容积可变的密闭容器中发生反应 | 正反应速率加快,逆反应速率不变 |
A. AB. BC. CD. D