题目内容
【题目】某兴趣小组的同学向一定体积的Ba(OH)2溶液中逐滴加入稀硫酸,并测得混合液的导电能力随时间变化曲线如图,该小组同学据图分析错误的是
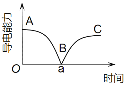
A.AB段溶液的导电能力不断减弱,说明电解质逐渐转变为非电解质
B.B处的导电能力为0,说明溶液中几乎没有自由移动的离子
C.BC段溶液的导电能力不断增大,主要是由于过量的Ba(OH)2电离出的离子导电
D.a时刻Ba(OH)2溶液中与稀硫酸恰好完全中和
【答案】AC
【解析】
A. AB段的反应为Ba(OH)2+H2SO4=BaSO4↓+2H2O,BaSO4、H2O都是电解质,故A错误;
B. 溶液导电的原因是有自由移动的离子,B处的导电能力为0,说明溶液中几乎没有自由移动的离子,故B正确;
C. BC段溶液的导电能力不断增大,主要是由于过量的稀硫酸电离出的离子导电,故C错误;
D. B处的导电能力为0,说明溶液中几乎没有自由移动的离子,Ba(OH)2溶液与稀硫酸恰好完全中和,故D正确;
选AC。

练习册系列答案
相关题目