题目内容
【题目】I.橙红色化合物A由五种元素组成,其中一种元素为原子半径最大的短周期元素(稀有气体元素除外),按如图流程进行实验。气体B为纯净物,能使湿润的红色石蕊试纸变蓝,溶液C呈黄色,沉淀D为砖红色沉淀。
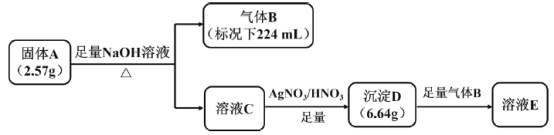
请回答:
(1)组成A的金属元素是___________(填元素符号),A的化学式是___________。
(2)沉淀D与足量B反应的离子反应方程式____________。
(3)A中的某种金属元素对应的单质可以通过铝热反应制备,写出化学反应方程式________。
II.某兴趣小组为了探究84消毒液(主要成分NaClO)和酒精混合使用是否存在安全隐患,利用如图装置进行实验。
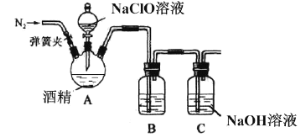
请回答:
(1)三颈烧瓶中出现黄绿色气体,请写出相应的化学方程式__________。(乙醇被氧化为乙醛)
(2)有同学用手触碰三颈烧瓶后发现,反应一段时间后装置温度升高,所以提出产生的气体中可能混有O2,请用离子方程式解释__________,该同学为了验证O2,打开弹簧夹,用带火星的木条检验,该操作的错误为___________。
【答案】Na 、Cr NH4NaCr2O7 Ag2CrO4+4NH3=2Ag(NH3)2++CrO42- Cr2O3+2Al![]() Al2O3+2Cr 2NaClO+C2H5OH→2NaOH+CH3CHO+Cl2↑ 2ClO-=O2+2Cl- 乙醇易挥发且易燃,与带火星木条存在安全隐患
Al2O3+2Cr 2NaClO+C2H5OH→2NaOH+CH3CHO+Cl2↑ 2ClO-=O2+2Cl- 乙醇易挥发且易燃,与带火星木条存在安全隐患
【解析】
I.根据流程短周期中原子半径最大的是金属钠,和氢氧化钠反应,生成能使湿润的红色石蕊试纸变蓝的气体,说明有NH4+;A为橙红色化合物且由五种元素组成,A与足量NaOH反应得到的溶液C呈黄色,溶液C与AgNO3/HNO3反应得到的沉淀D为砖红色沉淀,说明C含CrO42-,可知A中还含有Cr2O72-,沉淀D是Ag2CrO4;结合数据计算分析。
II.84消毒液具有强氧化性,酒精具有还原性,会发生氧化还原反应,产生的黄绿色气体是氯气,次氯酸根不稳定,易分解成氧气和氯离子。
I.(1)根据流程短周期中原子半径最大的是金属钠,和氢氧化钠反应,生成能使湿润的红色石蕊试纸变蓝的气体,说明有NH4+;A为橙红色化合物且由五种元素组成,A与足量NaOH反应得到的溶液C呈黄色,溶液C与AgNO3/HNO3反应得到的沉淀D为砖红色沉淀,说明C含CrO42-,可知A中还含有Cr2O72-,沉淀D是Ag2CrO4;组成A的金属元素是Na和Cr;根据N守恒,n(NH4+)=n(NH3)=0.224L÷22.4L/mol=0.01mol,根据Cr守恒,n(Cr2O72-)=![]() n(Ag2CrO4)=
n(Ag2CrO4)=![]() ×
×![]() =0.01mol,则n(Na+)=
=0.01mol,则n(Na+)=![]() =0.01mol,n(Na+):n(NH4+):n(Cr2O72-)=1:1:1,则A的化学式是NH4NaCr2O7,故本题答案:Na 、Cr;NH4NaCr2O7。
=0.01mol,n(Na+):n(NH4+):n(Cr2O72-)=1:1:1,则A的化学式是NH4NaCr2O7,故本题答案:Na 、Cr;NH4NaCr2O7。
(2)沉淀D是Ag2CrO4,和足量的氨气反应,沉淀溶解,发生的反应是:Ag2CrO4+4NH3=2Ag(NH3)2++CrO42-,故本题答案为:Ag2CrO4+4NH3=2Ag(NH3)2++CrO42-。
(3)铝热反应是利用铝的还原性制备高熔点、还原性比Al弱的金属,可制备金属铬,化学反应方程式为:Cr2O3+2Al![]() Al2O3+2Cr,故本题答案为:Cr2O3+2Al
Al2O3+2Cr,故本题答案为:Cr2O3+2Al![]() Al2O3+2Cr。
Al2O3+2Cr。
II.(1)84消毒液具有强氧化性,酒精具有还原性,会发生氧化还原反应,乙醇被氧化成乙醛,黄绿色气体是氯气,根据得失电子守恒、原子守恒,反应的化学方程式为2NaClO+C2H5OH→2NaOH+CH3CHO+Cl2↑,故本题答案为:2NaClO+C2H5OH→2NaOH+CH3CHO+Cl2↑。
(2)反应一段时间后装置温度升高,次氯酸根分解,有O2产生,离子方程式为2ClO-=O2+2Cl-;乙醇易挥发且易燃,所得气体中混有乙醇蒸气,用带火星的木条检验存在安全隐患,故本题答案为:2ClO-=O2+2Cl-;乙醇易挥发且易燃,与带火星木条存在安全隐患。

 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案【题目】某化学小组用50ml 0.50mol/L NaOH溶液和30ml 0.50mol/L硫酸溶液进行中和热的测定实验。
(1)实验中大约要使用230mL NaOH溶液,配制溶液时至少需要称量NaOH固体__ g。
(2)做中和热的测定实验时:桌上备有大、小两个烧杯、泡沫塑料、硬纸板、胶头滴管、环形玻璃搅拌棒.实验尚缺少的玻璃仪器(用品)是______、______。
(3)他们记录的实验数据如下:
①请填写表中的空白:
实验次数 | 起始温度t1 | 终止温度t2/℃ | 温度差平均值(t2﹣t1)/℃ | |
H2SO4 | NaOH | |||
1 | 25.0℃ | 25.0℃ | 29.1 | Δt=________ |
2 | 25.0℃ | 25.0℃ | 29.8 | |
3 | 25.0℃ | 25.0℃ | 28.9 | |
4 | 25.0℃ | 25.0℃ | 29.0 | |
②已知:溶液的比热容c为4.18 J·℃-1·g-1,溶液的密度均为1 g·cm-3。写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式____________(用该实验的数据,取小数点后一位)。
(4)若用氨水代替NaOH做实验,测定结果ΔH会___(填“偏大”、“偏大”、“无影响”)。