��Ŀ����
�����й�˵����ȷ����
| A��NH4Cl(s)��NH3(g)+HCl(g)�����²����Է����У�˵���÷�Ӧ�Ħ�H��0 |
| B����п����Ʒ�Ʋ����������Ʒ������ǰ���������⣬�����������෴ |
C������N2(g)+3H2(g) 2NH3(g)����������������ʱ��ѹ���������ʹѹǿ��������Ӧ���淴Ӧ�����Լ�H2��ƽ��ת���ʾ����� 2NH3(g)����������������ʱ��ѹ���������ʹѹǿ��������Ӧ���淴Ӧ�����Լ�H2��ƽ��ת���ʾ����� |
| D��100��ʱˮ�����ӻ�����KwΪ5.5��10��13��˵��ˮ�ĵ����Ƿ��ȷ�Ӧ |
C
�������������A���жϷ�Ӧ�ܷ��Է��������Ǧ�H�릤S������H��0�Ҧ�S��0��Ӧ���Է����У�����B���绯ѧ������ԭ��ص������õ����������ֺϽ��ж�п����Ʒ�������������յ������������������Ǹ�������ʴ�ӿ죬����C����ȷ��D���¶ȸ�ˮ�����ӻ����ˮ�ĵ��������ȷ�Ӧ������
���㣺���黯ѧ��Ӧԭ���Ļ���֪ʶ��

����ȼ�շ�Ӧ�ķ�Ӧ�Ȳ���ȼ���ȵ���
��H2(g)��O2(g)=H2O(l) ��H1 ��C(s)��O2(g)=CO(g) ��H2
��S(s)��O2(g)=SO2(g) ��H3 ��2H2S(g)��3O2(g)=2SO2(s)��2H2O(l) ��H4
| A���٢� | B���ڢ� | C���ڢ� | D���٢� |
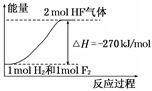
��֪��H2(g) �� F2(g) = 2HF(g) ��H��? 270 kJ/mol������˵����ȷ����
| A������ͬ�����£�1 mol H2��1 mol F2�������ܺʹ���2 mol HF��������� |
| B��1 mol H2��1 mol F2��Ӧ����2 molҺ̬HF�ų�������С��270 kJ |
| C���÷�Ӧ���淴Ӧ�Ƿ��ȷ�Ӧ |
| D���÷�Ӧ���̵������仯������ͼ����ʾ |
2HI(g)  H2(g)+I2(g)��Ӧ�����������仯��ͼ��ʾ(ͼ��E1��ʾ����Ӧ�Ļ�ܣ�E2��ʾ�淴Ӧ�Ļ��)�������й�������ȷ����
H2(g)+I2(g)��Ӧ�����������仯��ͼ��ʾ(ͼ��E1��ʾ����Ӧ�Ļ�ܣ�E2��ʾ�淴Ӧ�Ļ��)�������й�������ȷ����
| A���÷�ӦΪ���ȷ�Ӧ |
| B�������¶ȣ���Ӱ�����Ӱٷ��� |
| C�������ܽ��÷�Ӧ�Ļ�� |
| D���淴Ӧ�Ļ�ܵ�������Ӧ�Ļ�� |
������������ȷ����
| A�������������ڿ�������ѧ��ʴ�����䰵 |
| B������ȼ�ϵ����һ�ֽ���ѧ��ת��Ϊ���ܵ�װ�� |
| C�����ý������Ը��������Һ����ֽ������������������Ư���� |
| D�����ϴ���ȫ��ʧ�衱���г�ʹ�ó�Ϊ���У�����Ϊ���ϴ�����ռ�����أ������Խ��� |
���й�������ת������ʶ�У�����ȷ���ǣ� ��
| A���׳�ƹ���ʱ������ת��Ϊ��ѧ�� |
| B����ɫֲ����й������ʱ��̫����ת��Ϊ��ѧ�� |
| C�����ˮ��������������������ת��Ϊ��ѧ�� |
| D��úȼ��ʱ��ѧ����Ҫת��Ϊ���� |
�������������Ȼ�ѧ����ʽ��
H2��g��+ 1/2 O2(g) = H2O(g) �� ��H��a kJ/mol
H2��g��+ 1/2 O2(g) =H2O(l) �� ��H��b kJ/mol
2 H2��g��+ O2(g) ="2" H2O(l) �� ��H��c kJ/mol
���й������ǵı�����ȷ����( )
| A�����Ƕ������ȷ�Ӧ | B��a��b��c��Ϊ��ֵ |
| C����Ӧ�ȵĹ�ϵ��a=b | D����Ӧ�ȵĹ�ϵ��2b=c |
 CO2(g); ��H=��395.5 kJ��mol-1
CO2(g); ��H=��395.5 kJ��mol-1