题目内容
17.有机物A含碳54.5%、氢9.10%、氧36.4%(质量分数),在标准状况下,蒸气密度是1.96g•L-1它易溶于水,其水溶液与新制的氢氧化铜混合,加热到沸腾,有红色沉淀生成.有机物B含碳60%、氢13.33%、氧26.67%(质量分数),蒸气密度是氢气的30倍,它能发生酯化反应.则下列各组中,A、B的结构简式正确的( )| A. | CH3CHO HCOOCH3 | B. | CH3CH2CHO CH3COOH | ||
| C. | CH3CHO CH3COOH | D. | CH3CHO CH3CH(OH)CH3 |
分析 根据M=ρVm计算出有机物A的摩尔质量,再结合A分子中C、H、O的含量确定其分子式,水溶液与新制的氢氧化铜混合,加热到沸腾,有红色沉淀生成,说明A分子中含有醛基;密度与摩尔质量成正比,根据相对氢气的密度计算出B的相对分子量,再根据各元素含量确定B的分子,B能发生酯化反应,说明B分子中含有羧基或羟基,最后结合选项进行判断.
解答 解:有机物A在标准状况下的蒸气密度是1.96g•L-1,则A的摩尔质量为:M=22.4L/mol×1.96g/L≈44,结合选项可知,相对分子量为44的应该为CH3CHO,故B错误;
B的蒸气密度是氢气的30倍,则B的相对分子量为:2×30=60,B能发生酯化反应,则B分子中含有羟基或羧基,故A错误;
B含碳60%,则B分子中含有C原子数为:$\frac{60×60%}{12}$=3,故C错误;
根据分析可知,满足条件的A、B分别为:CH3CHO、CH3CH(OH)CH3,
故选D.
点评 本题考查了有机物分子式、结构简式的确定,题目难度中等,注意掌握根据相对密度、密度计算有机物相对分子量的方法,明确排除法中解答题中的应用.

练习册系列答案
相关题目
7.除去NaCl中含有的Ca2+、Mg2+、SO42-、HCO3-等离子,通常采用以下四种试剂,加入试剂合理的操作顺序是( )
①Na2CO3
②BaCl2
③NaOH
④HCl.
①Na2CO3
②BaCl2
③NaOH
④HCl.
| A. | ①②③④ | B. | ③①②④ | C. | ④②①③ | D. | ③②①④ |
9.下列反应不属于取代反应的是( )
| A. | 苯与溴反应制溴苯 | |
| B. | 苯与浓硝酸在浓硫酸作用下制硝基苯 | |
| C. | 乙醇与乙酸的酯化反应 | |
| D. | 一定条件下苯与氢气反应制环己烷 |
6.甲烷是最简单的烷烃,乙烯是最简单的烯烃,下列物质或方法中,不能用来鉴别二者的是( )
| A. | 燃烧 | B. | NaOH溶液 | ||
| C. | 溴的四氯化碳溶液 | D. | 酸性高锰酸钾溶液 |

 .B存在同素异形现象,其中常用作消毒剂的是O3.(填化学式)
.B存在同素异形现象,其中常用作消毒剂的是O3.(填化学式) .
.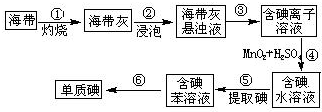 碘在工农业生产和日常生活中有重要用途.
碘在工农业生产和日常生活中有重要用途.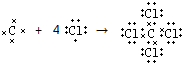 .
.