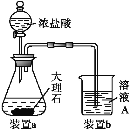
题目内容
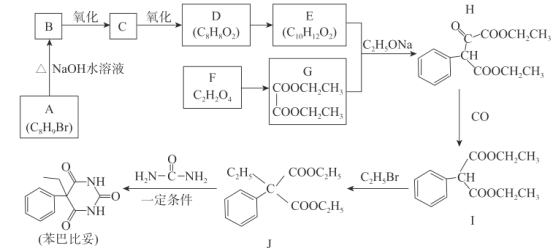
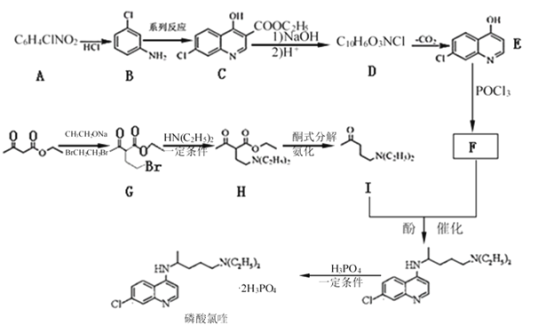
【题目】磷酸氯喹在细胞水平上能有效抑制新型冠状病毒2019-nCoV的感染。其中种以芳香化合物A 和乙酰乙酸乙酯(![]() )为原料合成磷酸氯喹的合成路线如图:
)为原料合成磷酸氯喹的合成路线如图:
已知:①![]() 具有酸性
具有酸性
②![]()
![]()
![]()
③R1NH2+R2X![]() R1NHR2+HX(X表示卤原子)。
R1NHR2+HX(X表示卤原子)。
请回答下列问题:
(1) E中含氧官能团的名称是________,G→H的反应类型是________。
(2)碳原子上连有4个不同的原子或基团时,该碳称为手性碳。写出B与足量的氢气加成后的产物M的结构简式,用星号(*)标出M中的手性碳_________。
(3) F的结构简式是_______。
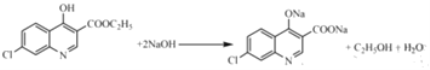
(4)写出C与NaOH反应的化学方程式为___________。
(5) N是H的同分异构体,符合下列条件的N的同分异构体共有____种: 写出其中一种核磁共振氢谱显示环上只有3组峰,且峰面积之比为4:4:1的结构简式________。
①含有基团![]() 、-N(C2H5)2
、-N(C2H5)2
②酸性水解产物中含有乙酸
③能与金属钠反应生成H2
(6)参照上述信息和合成路线,请设计以苯和1,4 -丁二醇为原料合成![]() 的合成路线(无机试剂任选)____________。
的合成路线(无机试剂任选)____________。
【答案】羟基 取代 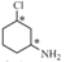
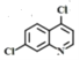
 19
19 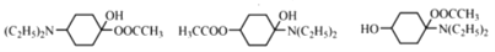 (任写一种)
(任写一种) 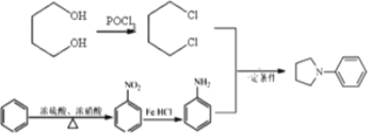
【解析】
根据已知信息②,在Fe/HCl的条件下-NO2发生还原转化为-NH2,B为间氨基氯苯,则A为间硝基氯苯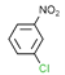 ;C中含有酚羟基与氢氧化钠发生酸碱中和,含有酯基发生碱性条件的水解,苯环上的氯原子性质稳定需要一定压强下可以水解,常温不与氢氧化钠反应,酸化后可以得到D
;C中含有酚羟基与氢氧化钠发生酸碱中和,含有酯基发生碱性条件的水解,苯环上的氯原子性质稳定需要一定压强下可以水解,常温不与氢氧化钠反应,酸化后可以得到D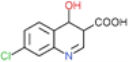 ,D经脱羧反应(-CO2)生成E,I和F发生信息③的反应,可知E结构中羟基被取代为氯原子,则F为
,D经脱羧反应(-CO2)生成E,I和F发生信息③的反应,可知E结构中羟基被取代为氯原子,则F为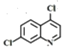 ;乙酰乙酸乙酯在乙醇钠的作用下与1,2-二溴乙烷发生取代反应,生成HBr和G,G与HN(C2H5)2在一定条件下取代反应(参考信息③),生成HBr和H,以此作答。
;乙酰乙酸乙酯在乙醇钠的作用下与1,2-二溴乙烷发生取代反应,生成HBr和G,G与HN(C2H5)2在一定条件下取代反应(参考信息③),生成HBr和H,以此作答。
(1) E中含氧官能团的名称是羟基;参考已知信息③,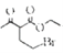 与HN(C2H5)2在一定条件下生成和
与HN(C2H5)2在一定条件下生成和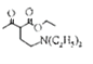 和HBr,故G→H的反应类型是取代反应;
和HBr,故G→H的反应类型是取代反应;
(2)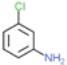 与足量的氢气加成后的产物M为
与足量的氢气加成后的产物M为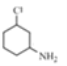 ,连接Cl原子的碳、连接N原子的碳均连接了四个不同基团,故为手性碳原子,可表示为
,连接Cl原子的碳、连接N原子的碳均连接了四个不同基团,故为手性碳原子,可表示为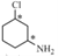 ;
;
(3)根据分析,F的结构简式是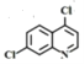 ;
;
(4)根据分析,C中含有酚羟基与NaOH发生酸碱中和,含有酯基在碱性条件下发生水解生成羧酸盐和乙醇,苯环上的氯原子稳定,需要在一定压强下才能反应,故C与NaOH反应的化学方程式为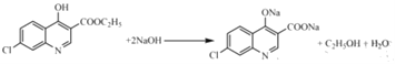 ;
;
(5)H的同分异构体N能水解且酸性水解产物含有乙酸,说明分子内含有CH3COO-,能与金属钠反应生成氢气,说明含有-OH,另已知分子含有含有![]() 和-N(C2H5)2;若CH3COO-、-OH、-N(C2H5)2连接
和-N(C2H5)2;若CH3COO-、-OH、-N(C2H5)2连接![]() 的不同碳原子上,同分异构体有10种(类似于苯环上ABC的10种结构);若两两基团连接相同碳原子(三种基团两两组合有三种情况),另外一个基团可以邻间对放置,则可得到9种同分异构体;根据上述分析符合条件的N的同分异构体共19种; 其中核磁共振氢谱显示环上只有3组峰,且峰面积之比为4:4:1,根据要求应该在两两组合中对位结构,故结构简式为
的不同碳原子上,同分异构体有10种(类似于苯环上ABC的10种结构);若两两基团连接相同碳原子(三种基团两两组合有三种情况),另外一个基团可以邻间对放置,则可得到9种同分异构体;根据上述分析符合条件的N的同分异构体共19种; 其中核磁共振氢谱显示环上只有3组峰,且峰面积之比为4:4:1,根据要求应该在两两组合中对位结构,故结构简式为![]() (任写一种);
(任写一种);
(6)根据产物结构分析,出现R1NR2R3需要运用信息③R1NH2+R2X![]() R1NHR2+HX,可知R1代表苯环,R2R3代表环状结构,需要在苯环上发生硝化反应,再被还原得苯胺,R2R3需要出现卤素原子,根据信息采用POCl3引入两个氯原子,然后发生类似于信息③反应进行合成,则路线为
R1NHR2+HX,可知R1代表苯环,R2R3代表环状结构,需要在苯环上发生硝化反应,再被还原得苯胺,R2R3需要出现卤素原子,根据信息采用POCl3引入两个氯原子,然后发生类似于信息③反应进行合成,则路线为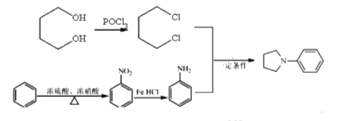 。
。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】研究CO和CO2的利用对促进低碳社会的构建具有重要意义。请回答下列问题:
(1)利用CO和H2在一定条件下可合成甲醇,发生反应: CO(g)+ 2H2(g)![]() CH3OH(g),其两种反应过程中能量的变化曲线如图中a、b所示,下列说法正确的是_____(填字母)。
CH3OH(g),其两种反应过程中能量的变化曲线如图中a、b所示,下列说法正确的是_____(填字母)。
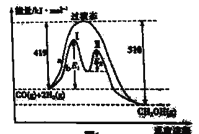
A.上述反应的△H= -91 kJ·mol-1
B.该反应自发进行的条件为高温
C. b过程使用催化剂后降低了反应的活化能和H
D. b过程的反应速率:第Ⅱ阶段>第Ⅰ阶段
(2)若反应CO(g)+2H2(g)![]() CH3OH(g)在温度不变且体积恒定为1L密闭容器中发生,反应过程中各物质的物质的量随时间变化见表所示:
CH3OH(g)在温度不变且体积恒定为1L密闭容器中发生,反应过程中各物质的物质的量随时间变化见表所示:
时间/min | 0 | 5 | 10 | 15 |
H2 | 4 | 2 | ||
CO | 2 | 1 | ||
CH3OH(g) | 0 | 0.7 |
①下列各项能作为判断该反应达到平衡标志的是_______(填字母)
A.2v正(H2)=v逆(CH3OH)
B. CO与CH3OH的物质的量之比保持不变
C.混合气的平均相对分子质量保持不变
D.混合气体的密度保持不变
②若起始压强为P0kPa,反应速率若用单位时间内分压的变化表示,则10 min内H2的反应速率v(H2)=_____kPa/min;该温度下反应的平衡常数Kp=______。(分压=总压×物质的量分数)。
(3)甲和乙两个恒容密闭容器的体积相同,向甲中加入1 mol CO和2 mol H2,向乙中加入2 mol CO和4 molH2,测得不同温度下CO的平衡转化率如图所示,则L、M两点容器内平衡常数:K(M)_____ K(L); 压强:p(M)__2p(L)。(填“>”“<”或“=”)

(4)以纳米二氧化钛为工作电极,稀硫酸为电解质溶液,在一定条件下通入CO2进行电解,在阴极可制得低密度聚乙烯(![]() )。电解时,阴极的电极反应式是_________。
)。电解时,阴极的电极反应式是_________。