题目内容
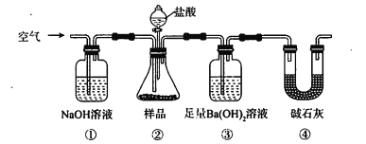
【题目】将0.20 mol NO和0.20 mol CO混合气体充入容积为2.0 L的恒容密闭容器中,分别在T1和T2温度下发生反应:2NO(g)+2CO(g)![]() N2(g)+2CO2(g)。反应过程中容器内CO2的物质的量随时间变化关系如图所示,下列说法正确的是
N2(g)+2CO2(g)。反应过程中容器内CO2的物质的量随时间变化关系如图所示,下列说法正确的是
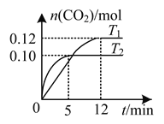
A.T1<T2
B.容器内气体的密度不再改变时反应到达平衡
C.T2温度下,该反应的平衡常数K=10
D.T1温度时,前12 min的平均反应速率v(CO)=0.01 mol·L-1·min-1
【答案】AC
【解析】
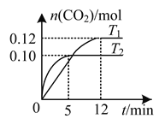
A. 由图T2先达到平衡,对应温度高,T1<T2,故A正确;
B. 气体的质量不变,体积不变,容器内气体的密度不再改变时,不能判断反应是否到达平衡,故B错误;
C. T2温度下,2NO(g)+2CO(g)![]() N2(g)+2CO2(g)
N2(g)+2CO2(g)
起始量/mol 0.2 0.2
变化量/mol 0.1 0.1 0.05 0.1
平衡量/mol 0.1 0.1 0.05 0.1
该反应的平衡常数K=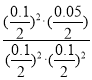 =10,故C正确;
=10,故C正确;
D. T1温度时,前12 min的平均反应速率v(CO)=(0.2-0.12)mol÷2L÷12min=0.003 33mol·L-1·min-1,故D错误;
故选AC.

 应用题作业本系列答案
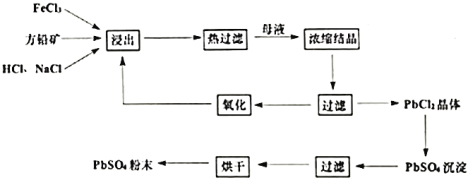
应用题作业本系列答案【题目】随着新能源汽车产业的快速发展,带来大量的废旧电池,一种以废旧磷酸铁锂电池正极为原料回收铝、铁和锂元素的工艺流程如下:
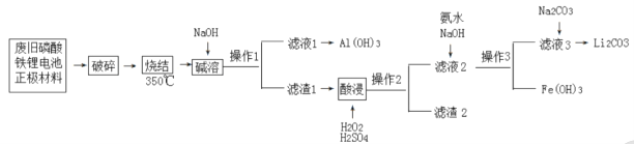
已知:①![]() 易溶于硫酸中。
易溶于硫酸中。
②磷酸铁锂电池正极材料:磷酸铁锂![]() ,乙炔黑(主要成分碳单质,着火点大于750℃)导电剂和有机粘结剂PVDF(一种高分子有机物),均匀混合后涂覆于铝箔上。
,乙炔黑(主要成分碳单质,着火点大于750℃)导电剂和有机粘结剂PVDF(一种高分子有机物),均匀混合后涂覆于铝箔上。
回答下列问题:
(1)破碎的作用是________,烧结的主要目的是________。
(2)碱溶发生的非氧化还原反应的离子方程式是________________。
(3)若在实验室中进行操作1、2、3,需要用到的玻璃仪器有________。
(4)滤渣1酸浸的目的是________。
(5)滤渣2主要成分是________。
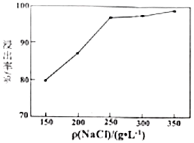
(6)pH与Fe、Li沉淀率关系如下表,为使滤液2中Fe、Li分离,溶液的pH应调节为________。
溶液pH与Fe、Li沉淀率关系
pH | 3.5 | 5 | 6.5 | 8 | 10 | 12 |
Fe沉淀率 | 66.5 | 79.2 | 88.5 | 97.2 | 97.4 | 98.1 |
Li沉淀率 | 0.9 | 1.3 | 1.9 | 2.4 | 4.5 | 8.0 |
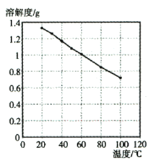
(7)碳酸锂的溶解度随温度变化如下图所示。向滤液3中加入![]() ,将温度升至90℃是为了提高沉淀反应速率和________。
,将温度升至90℃是为了提高沉淀反应速率和________。
【题目】下列各组实验操作、现象、解释或结论均正确的是( )。
操作 | 现象 | 解释或结论 | |
A | 将石蜡油蒸汽通过炽热的碎瓷片产生的气体通入溴的四氯化碳溶液 | 溴的四氯化碳溶液逐渐褪色 | 烷烃分解产生的烯烃与溴发生了氧化反应 |
B | 将螺旋状铜丝在酒精灯上灼烧至红热插入乙醇中 | 铜丝恢复光亮的紫红色且可闻到刺激性气味 | 铜丝做催化剂,乙醇被氧化成乙醛 |
C | 将乙醇、乙酸、浓硫酸混合共热产生的蒸汽通到饱和 | 液面上有透明的不溶于水的油状液体生成,并可以闻到香味 | 浓硫酸做催化剂、加热条件下,乙醇和乙酸发生了酯化反应 |
D | 蔗糖溶液加少许稀硫酸后水浴加热几分钟,然后取少量溶液加入新制 | 未见砖红色沉淀产生 | 蔗糖尚未水解 |
A.AB.BC.CD.D