题目内容
【题目】在恒温、恒容的容器中进行反应:2HI![]() H2+I2(正反应为吸热反应),反应物的浓度由0.1 mol/L降到0.06 mol/L需要20 s,那么由0.06 mol/L降到0.036 mol/L所需时间为
H2+I2(正反应为吸热反应),反应物的浓度由0.1 mol/L降到0.06 mol/L需要20 s,那么由0.06 mol/L降到0.036 mol/L所需时间为
A. 等于10 s B. 等于12 s C. 大于12 s D. 小于12 s
【答案】C
【解析】试题反应物的浓度由0.1 mol·L-1降到0.06 mol·L-1需20 s,其反应速率为0.002 mol·L-1·s-1,若由0.06 mol·L-1降到0.036 mol·L-1,假设反应速率不变,设反应所需时间为x,根据化学反应速率的计算公式得,(0.06mol/L-0.036mol/L)÷x=0.002mol·L-1·s-1,解得x=12s,实际上,随着反应的进行,反应物浓度逐渐降低,反应速率逐渐减小,所需的时间会大于12s,答案选C。

练习册系列答案
 期末集结号系列答案
期末集结号系列答案
相关题目
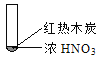
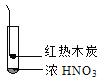
【题目】下述实验中均有红棕色气体产生,对比分析所得结论不正确的是
|
|
|
① | ② | ③ |
A. 由①中的红棕色气体,推断产生的气体一定是混合气体
B. 红棕色气体不能表明②中木炭与浓硝酸发生了反应
C. ③的气体产物中检测出CO2,说明木炭一定与浓硝酸发生了反应
D. 由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物