��Ŀ����
5����ͼ�ǽ���ͭ��Ũ���ᷴӦ�����в�������װ�ã���l�� A �Թ��ڷ�����Ӧ�Ļ�ѧ����ʽ��Cu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O��
��2����Ӧ��A �Թ��е�Һ��������ˮϡ�ͺ�����ɫ��
B �Թ���Ʒ����Һ����ɫ����Ϊ��ɫ��
��3��C�Թ�������������Һ�����������ն����SO2����ֹ������Ⱦ�����ӷ�Ӧ����ʽΪSO2+2OH-=SO32-+H2O��
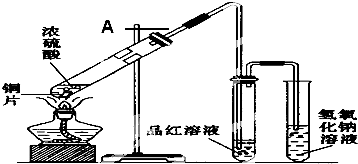
���� ��1��A�Թ���ͭ��Ũ������ȷ�Ӧ��������ͭ�����������ˮ���ݴ�д����Ӧ�Ļ�ѧ����ʽ��
��2��ͭ��Ũ���ᷴӦ����������ͭ����Ӧ�����Һϡ�ͺ���Һ��ʾ��ɫ����Ӧ���ɵĶ��������������Ư���ԣ��ܹ�ʹƷ����Һ��ɫ��
��3�����������ж�����Ҫʹ������������Һ����δ��Ӧ�Ķ�������������������������Һ��Ӧ�����������ƺ�ˮ���ݴ�д����Ӧ�����ӷ���ʽ��
��� �⣺��1��ͭ��Ũ���ᷴӦ��������ͭ�����������ˮ����Ӧ�Ļ�ѧ����ʽΪ��Cu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O��
�ʴ�Ϊ��Cu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O��
��2����Ӧ��A�Թ��е�Һ���к�������ͭ��������ˮϡ�ͺ�����ɫ��ͭ��Ũ���ᷴӦ�����˾���Ư���ԵĶ�����������B�Թ���Ʒ����Һ��ɫ�����ɺ�ɫ��Ϊ��ɫ��
�ʴ�Ϊ��������ɫ��
��3����������Ϊ�ж����壬��Ҫ����β�����գ�C������������Һ�����������ն����SO2����ֹ������Ⱦ����������������������Һ��Ӧ�����ӷ���ʽΪ��SO2+2OH-=SO32-+H2O��
�ʴ�Ϊ�����ն����SO2����ֹ������Ⱦ��SO2+2OH-=SO32-+H2O��
���� ���⿼������Ũ����Ļ�ѧ���ʣ���Ŀ�ѶȲ���ע������ͭ��Ũ����ķ�Ӧԭ������������ļ��鷽����������ػ���֪ʶ�Ŀ��飬���������ѧ�����Ӧ�û���֪ʶ��������

 ���ɿ��õ�Ԫ������ĩר����100��ϵ�д�
���ɿ��õ�Ԫ������ĩר����100��ϵ�д�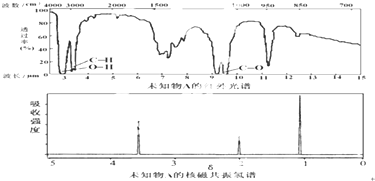
| A�� | �ɺ������֪�����л��������������ֲ�ͬ�Ļ�ѧ�� | |
| B�� | �ɺ˴Ź�������֪�����л�������������ֲ�ͬ��ѧ��������ԭ�� | |
| C�� | ������˴Ź�����������֪������е���ԭ������ | |
| D�� | ��A�Ļ�ѧʽΪC3H6O������ṹ��ʽΪCH3COCH3 |
| A�� | ��ϵͳ��������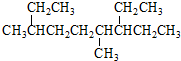 ������Ϊ3��6-����-7-�һ����� ������Ϊ3��6-����-7-�һ����� | |
| B�� | 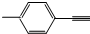 ����������ԭ�ӹ�ƽ�� ����������ԭ�ӹ�ƽ�� | |
| C�� | ��״���£�1 L������ȫȼ������CO28L | |
| D�� | 1.0 mol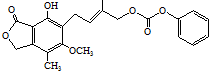 �������5.0 mol NaOHˮ��Һ��ȫ��Ӧ �������5.0 mol NaOHˮ��Һ��ȫ��Ӧ |
| A�� | ��������������������� | |
| B�� | ����������ˮ�ķ�Ӧ��������ԭ��Ӧ | |
| C�� | ��������������ɴ�����Ⱦ������֮һ | |
| D�� | ��ͨ��״���²�õ�NO2����Է��������Dz�ȷ�� |
| A�� | �ô�������β���е�CO��NO��CO+NO$\frac{\underline{\;����\;}}{\;}$C+NO2 | |
| B�� | ����SO2ͨ�뵽Ba��OH��2��Һ��SO2+Ba2++2OH-�TBaSO3��+H2O | |
| C�� | NH4HCO3���ڹ�����NaOH��Һ�У�HCO3+OH-�TCO32-+H2O | |
| D�� | Ũ������������̹��ȣ�Mn2O+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$Mn2++2Cl-+Cl2��+2H2O |
H+��aq��+OH-��aq���TH2O��l����H=-57.3kJ•mol-1
��֪��CH3COOH��aq��+NaOH��aq���TCH3COONa��aq��+H2O��l����H=-Q1 kJ•mol-1
HNO3��aq��+NaOH��aq���TNaNO3��aq��+H2O��l����H=-Q2 kJ•mol-1
CH3COOH��aq��+NH3•H2O��aq���TCH3COONH4��aq��+H2O��l����H=-Q3 kJ•mol-1
������������Һ�н��еķ�Ӧ��Q1��Q2��Q3�Ĺ�ϵ��ȷ���ǣ�������
| A�� | Q1=Q2=Q3=57.3 | B�� | Q1��Q2��Q3��57.3 | C�� | Q3��Q1��Q2=57.3 | D�� | ��ȷ�� |

����˵����ȷ���ǣ�������
| A�� | ��ɫ��������Al��OH��3���������CO2��ԭ�������һ������Al3+��HCO3- | |
| B�� | ��ɫ��������BaSO4��ԭ�������һ������SO42- | |
| C�� | ������һ����NO��NO2�Ļ������ | |
| D�� | ԭ�������һ������Na+��Al3+��NO3-��SO32- |