题目内容
5.以元素化合价升降的观点分析下列各化学反应,其中不属于氧化还原反应的是( )| A. | Mg+2HCl═MgCl2+H2↑ | B. | H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl | ||
| C. | CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O | D. | CaCl2+Na2CO3═CaCO3↓+2NaCl |
分析 如发生氧化还原反应,则一定存在元素化合价的升降,根据反应前后元素的化合价是否发生变化解答该题.
解答 解:A.Mg、H元素化合价发生变化,属于氧化还原反应,故A不选;
B.H、Cl元素化合价发生变化,属于氧化还原反应,故B不选;
C.Cu、H元素化合价发生变化,属于氧化还原反应,故C不选.
D.为复分解反应,元素化合价没有发生变化,故D选.
故选D.
点评 本题考查氧化还原反应,为高频考点,侧重于基本概念的考查,注意把握氧化还原反应的特征以及元素化合价,难度不大.

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目
8.下列关于化学用语的理解正确的是( )
| A. | 比例模型 表示甲烷分子或四氯化碳分子 表示甲烷分子或四氯化碳分子 | |
| B. | 乙醛的结构简式为CH3CH2OH | |
| C. | Cl-离子的结构示意图: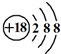 | |
| D. | “84消毒液”中有效成分NaClO的电子式为: |
16.下列关于物质用途的描述中错误的是( )
| A. | 钾钠合金可以用于快中子反应堆的热交换剂 | |
| B. | MgO是优质的耐高温材料 | |
| C. | 铝合金密度小、强度高,可制成汽车车轮骨架和飞机构件 | |
| D. | 用钠和氯气反应制备氯化钠 |
13.已知A为烃,B是烃的衍生物,由总物质的量为1mol的A和B组成的混合物在2.5mol氧气中完全燃烧,生成2mol二氧化碳和2mol水.A、B分子式不可能是下列组合中的( )
| A. | CH4O、C3H4O | B. | C2H4、C2H4O2 | C. | C3H6O3、CH2O2 | D. | C2H2、C2H6 |
20.2SO2(g)+O2(g)$\frac{\underline{\;V_{2}O_{5}\;}}{△}$2S03(g)是制备硫酸的重要反应之一.下列叙述正确的是( )
| A. | 催化剂V2O5,不改变该反应的逆反应速率 | |
| B. | 将2 mol SO2与2 mol O2放人密闭容器中,最终生成2mol SO3 | |
| C. | 在t1、t2时刻,SO2(g)的浓度分别是C1、C2,则时间间隔t1-t2内,SO2(g)消耗的平均速率为v=$\frac{{C}_{1}-{C}_{2}}{{t}_{2}-{t}_{1}}$ | |
| D. | 该反应是放热反应,则SO2的能量一定大于SO3的能量 |
10.硒有两种同素异形体:灰硒和红硒.灰硒溶于三氯甲烷,红硒溶于二硫化碳,它们都不溶于水,则灰硒和红硒的晶体属于( )
| A. | 原子晶体 | B. | 分子晶体 | C. | 金属晶体 | D. | 以上均有可能 |
17.下列物质中能与钠、氢氧化钠、碳酸氢钠都反应的是( )
| A. | 苯酚 | B. | CH3COOCH2CH2CH3 | C. | HCOOH | D. | CH3OH |
14.下列化学用语正确的是( )
| A. | 醛基的电子式: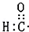 | B. | 三硝基甲苯的结构简式: | ||
| C. | 丙烷分子的比例模型: | D. | 2-乙基-1,3-丁二烯的键线式: |
15.下列分子中所有原子都满足最外层为8电子结构的是( )
①BeCl2 ②NCl3 ③PCl5 ④COCl2 ⑤SF6 ⑥XeF2 ⑦CS2 ⑧CH4 ⑨CF2Cl2⑩S2Cl2.
①BeCl2 ②NCl3 ③PCl5 ④COCl2 ⑤SF6 ⑥XeF2 ⑦CS2 ⑧CH4 ⑨CF2Cl2⑩S2Cl2.
| A. | ②④⑦⑧⑨⑩ | B. | ②④⑦⑨⑩ | C. | ③④⑦⑩ | D. | ④⑤⑦⑨⑩ |