��Ŀ����
����Ŀ��ij��ѧ��ȤС��Ϊ��̽��̼�����ϡ���ᷴӦ�����е����ʱ仯����VmLϡ�����м���������̼��ƣ��ռ���Ӧ�ų���CO2����������ѻ���Ϊ��״���µ���ֵ����ʵ���¼���£��ۼ�ֵ����
ʱ�䣨min�� | 1 | 2 | 3 | 4 | 5 |
CO2�����mL�� | 50 | 120 | 232 | 290 | 310 |
��1��0��1 min��1��2 min��2��3 min��3��4 min��4��5 min���ʱ����У�_________��Ӧ������졣
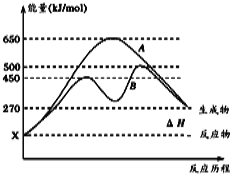
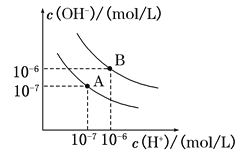
��2��������Һ������䣬4��5minʱ����������Ũ�ȱ仯����ʾ�ĸ÷�Ӧ����Ϊ____________________________��
��3��Ϊ�˽���������ѧ��Ӧ�ķ�Ӧ���ʣ�����Һ�м����������ʣ�����Ϊ���е���
_______________�����ţ���
a������ˮ b��Ũ���� c��NaCl���� d��NaCl��Һ
��4���������������⣬����Ϊ�����Բ�ȡ��Щ��ʩ�����ͻ�ѧ��Ӧ���ʣ�����д������_______________________________________________________________________��
________________________________________________________________________��
���𰸡� 2��3 min 1/560v mol��L-1��min-1 a��d ���ͷ�Ӧ�¶� ���ٽӴ����
���������ɱ������ݿ�֪��0��1��1��2��2��3��3��4��4��5min���������ֱ�Ϊ50mL��70mL��112mL��58mL��20mL��
(1)2 min��3 min�ռ�������������ʱ��ζ࣬��Ӧ���������÷�Ӧ���ȣ��¶����ӿ췴Ӧ�����йأ��ʴ�Ϊ��2��3 min��
(2)��4��5minʱ����ڣ����ɱ���¶�����̼�����Ϊ��20mL��n(CO2)= ![]() =
= ![]() mol����2HCl��CO2��֪��������������ʵ���Ϊ
mol����2HCl��CO2��֪��������������ʵ���Ϊ![]() mol�����(HCl)=
mol�����(HCl)= 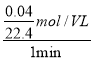 =
=![]() mol/(Lmin)���ʴ�Ϊ��
mol/(Lmin)���ʴ�Ϊ�� ![]() mol/(Lmin)��
mol/(Lmin)��
(3)a����������ˮ�������Ũ�ȼ�С����Ӧ���ʼ�������ȷ��b������Ũ���ᣬ�����Ũ������Ӧ���ʼӿ죬����c������NaCl���壬�����Ũ�Ȳ��䣬��Ӧ���ʲ��䣬����d��NaCl��Һ ���൱��ϡ�����ᣬ�����Ũ�ȼ�С����Ӧ���ʼ�������ȷ����ѡad��
(4)Ҫ����̼��ƺ�����Ļ�ѧ��Ӧ���ʣ����Ը���Ӱ�컯ѧ��Ӧ���ʵ����ؿ��ǣ��罵�ͷ�Ӧ�¶������ٽӴ�����ȣ��ʴ�Ϊ�����ͷ�Ӧ�¶ȡ����ٽӴ������

 ѧ�����νӽ̲��Ͼ���ѧ������ϵ�д�
ѧ�����νӽ̲��Ͼ���ѧ������ϵ�д� Сѧ������ҵϵ�д�
Сѧ������ҵϵ�д� ��ʿһ��ȫͨϵ�д�
��ʿһ��ȫͨϵ�д�����Ŀ����һ�ܱ�������ͨ��A��B��C�������壬����һ���¶ȣ���t1��t4 sʱ��ø����ʵ�Ũ��������������ж���ȷ����( )
�ⶨʱ��/s Ũ�� | t1 | t2 | t3 | t4 |
c(A)/(mol��L��1) | 6 | 3 | 2 | 2 |
c(B)/(mol��L��1) | 5 | 3.5 | 3 | 3 |
c(C)/(mol��L��1) | 1 | 2.5 | 3 | 3 |
A. ��t3 sʱ��Ӧ�Ѿ�ֹͣ
B. t3��t4 s�������淴Ӧ���ʲ����
C. �������з����ķ�ӦΪA(g)��B(g) C(g)
D. ��t2��t3 s��A��ƽ����Ӧ����Ϊ![]() mol/(L��s)
mol/(L��s)