题目内容
【题目】通常条件下,下列物质能用化合反应制得的是
A.![]() B.
B.![]() C.
C.![]() D.CuS
D.CuS
【答案】B
【解析】
两种或两种以上的物质反应生成一种物质的反应为化合反应。
A.可通过可溶性的铝盐和碱发生复分解反应生成氢氧化铝;
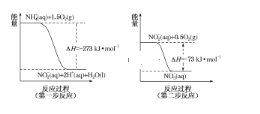
B.氢氧化亚铁和氧气、水反应生成氢氧化铁;
C.利用强酸制取弱酸的原理制备硅酸;
D.硫和铜反应生成硫化亚铜。
![]() 制备氢氧化铝,可用铝盐和氨水反应,离子反应为:
制备氢氧化铝,可用铝盐和氨水反应,离子反应为:![]() ,属于复分解反应,无法以化合反应制取,故A错误;
,属于复分解反应,无法以化合反应制取,故A错误;
B.反应方程式为:![]() ,B可以实现,故B正确;
,B可以实现,故B正确;
C.制备硅酸的反应为:![]() ,是两种化合物相互交换成分生成另外两种化合物的反应,故为复分解反应,故C错误;
,是两种化合物相互交换成分生成另外两种化合物的反应,故为复分解反应,故C错误;
D.硫为弱氧化剂,则铜粉和硫粉混合加热制备硫化亚铜,无法通过化合反应制取硫化铜,故D错误;
故选:B。

【题目】平板电视显示屏生产过程中会产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2)。利用废玻璃粉末可以制取多种化工产品。设计流程如下:
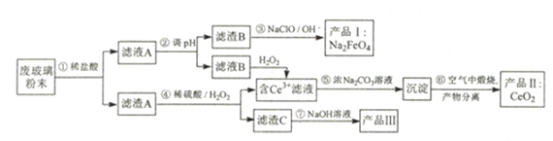
查阅资料可知:
①CeO2性质:淡黄或黄褐色粉末,不溶于水和碱,微溶于酸;有强氧化性。
②Ce3+在碱金属碳酸盐溶液中生成难溶的碳酸复盐Ce2(CO3):Na2CO3·2H2O。
③常温时两种沉淀物的溶度积见表:
沉淀物 | Fe(OH)3 | Ce(OH)3 |
Ksp | 4.0×10-38 | 1.5×10-20 |
回答下列问题:
(1)过程①分离操作中用到的玻璃仪器有_______________________________。
(2)过程④中发生反应的离子方程式为_________________________________,过程⑥中发生的化学反应方程式为__________________________________。
(3)产品I是一种新型、绿色的多功能净水剂,集氧化、灭菌、消毒、吸附、絮凝、沉淀等性能为一体。净水过程中,Na2FeO4 起到吸附、絮凝作用的原理是_________________。
(4)工业上也可用电解浓NaOH溶液制备产品I。用铁做电极,写出电解时阳极发生的电极反应方程式_________________。
(5)沉淀过程中,当某种离子浓度降至10—5 mol·L-1时,可认为此离子完全沉淀。过程②中Fe3+沉淀完全时溶液的pH=_____ (已知 lg2=0.3)。
(6)写出产品III的一种用途______________________________________。