题目内容
13.芳香族化合物C的分子式为C9H9OCl,C与其他物质之间的转化如图所示:C分子中有一个甲基且苯环上只有一条侧链;一定条件下C能发生银镜反应.
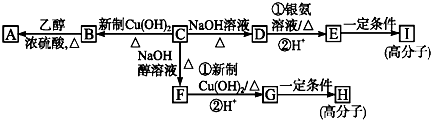
(1)F中含氧官能团的名称是醛基;CF的反应类型是消去反应.
(2)H的结构简式是
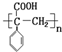 .
.(3)写出D与银氨溶液反应的化学方程式:
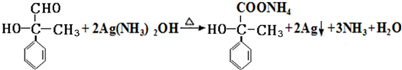 .
.(4)有的同学认为B中可能没有氯原子,你是同意(填“同意”或“不同意”),你的理由是在碱性环境中氯原子可能水解.
(5)D的一种同系物W(分子式为C8H8O2)有多种同分异构体,则符合以下条件的W的同分异构体有4种.
①属于芳香族化合物;
②遇FeCl3溶液不变紫色;
③能与NaOH溶液发生反应但不属于水解反应写出其中核磁共振氢谱有4个峰的结构简式:
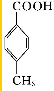 .
.
分析 芳香族化合物C的分子式为C9H9OC1,C分子中有一个甲基且苯环上只有一个侧链,C能和氢氧化钠的水溶液发生取代反应生成D,D能和银氨溶液发生银镜反应,则D中含有醛基和醇羟基,C的结构简式为: ,D的结构简式为:
,D的结构简式为: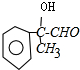 ,D和银氨溶液反应、酸化生成E,则E的结构简式为:
,D和银氨溶液反应、酸化生成E,则E的结构简式为: ,E发生酯化反应进行缩聚反应生成高聚物I,I为
,E发生酯化反应进行缩聚反应生成高聚物I,I为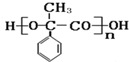 .C和氢氧化钠的醇溶液发生消去反应生成F,则F的结构简式为:
.C和氢氧化钠的醇溶液发生消去反应生成F,则F的结构简式为: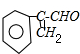 ,F被新制氢氧化铜氧化然后酸化生成G,G的结构简式为:
,F被新制氢氧化铜氧化然后酸化生成G,G的结构简式为: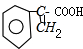 ,G发生加聚反应生成H,H的结构简式为:
,G发生加聚反应生成H,H的结构简式为: .C被新制氢氧化铜氧化生成B,然后酸化,则B的结构简式为:
.C被新制氢氧化铜氧化生成B,然后酸化,则B的结构简式为: ,B和乙醇发生酯化反应生成A,据此解答.
,B和乙醇发生酯化反应生成A,据此解答.
解答 解:芳香族化合物C的分子式为C9H9OC1,C分子中有一个甲基且苯环上只有一个侧链,C能和氢氧化钠的水溶液发生取代反应生成D,D能和银氨溶液发生银镜反应,则D中含有醛基和醇羟基,C的结构简式为: ,D的结构简式为:
,D的结构简式为: ,D和银氨溶液反应、酸化生成E,则E的结构简式为:
,D和银氨溶液反应、酸化生成E,则E的结构简式为: ,E发生酯化反应进行缩聚反应生成高聚物I,I为
,E发生酯化反应进行缩聚反应生成高聚物I,I为 .C和氢氧化钠的醇溶液发生消去反应生成F,则F的结构简式为:
.C和氢氧化钠的醇溶液发生消去反应生成F,则F的结构简式为: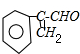 ,F被新制氢氧化铜氧化然后酸化生成G,G的结构简式为:
,F被新制氢氧化铜氧化然后酸化生成G,G的结构简式为: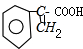 ,G发生加聚反应生成H,H的结构简式为:
,G发生加聚反应生成H,H的结构简式为: .C被新制氢氧化铜氧化生成B,然后酸化,则B的结构简式为:
.C被新制氢氧化铜氧化生成B,然后酸化,则B的结构简式为: ,B和乙醇发生酯化反应生成A,
,B和乙醇发生酯化反应生成A,
(1)F的结构简式为: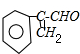 ,含氧官能团的名称是:醛基;C和氢氧化钠的醇溶液发生消去反应生成F,
,含氧官能团的名称是:醛基;C和氢氧化钠的醇溶液发生消去反应生成F,
故答案为:醛基;消去反应;
(2)由上述分析可知,H的结构简式为: ,
,
故答案为: ;
;
(3)D与银氨溶液反应的方程式为: ,
,
故答案为: ;
;
(4)在碱性环境中氯原子可能水解,B中可能没有氯原子,
故答案为:同意;在碱性环境中氯原子可能水解;
(5) 有多种同分异构体,则符合以下条件的同分异构体:①属于芳香族化合物,含有1个苯环;②遇FeCl3溶液不变紫色,不含酚羟基;③能与NaOH溶液发生反应但不属于水解反应,含有羧基-COOH,④只有一个-CH3,故可能可以1个侧链,为-CH(CH3)-COOH,可能可以2个侧链,为-CH3、-CH2COOH,有邻、间、对三种位置关系3种,共有4种,其中核磁共振氢谱有4个峰的结构简式为
有多种同分异构体,则符合以下条件的同分异构体:①属于芳香族化合物,含有1个苯环;②遇FeCl3溶液不变紫色,不含酚羟基;③能与NaOH溶液发生反应但不属于水解反应,含有羧基-COOH,④只有一个-CH3,故可能可以1个侧链,为-CH(CH3)-COOH,可能可以2个侧链,为-CH3、-CH2COOH,有邻、间、对三种位置关系3种,共有4种,其中核磁共振氢谱有4个峰的结构简式为 ,
,
故答案为:4; .
.
点评 本题考查了有机物的推断,明确有机物的官能团及其结构是解本题关键,充分利用题给信息采用正逆相结合的方法进行推断,难度中等.注意(5)条件同分异构体的书写.

 互动课堂系列答案
互动课堂系列答案| A. | 铝与氧化铁反应既是氧化还原反应,又是吸热反应 | |
| B. | 化学反应中的能量变化只体现为热量的形式 | |
| C. | Ca O+H2O=Ca (OH)2反应过程中,旧键断裂吸收的能量小于新键形成释放的能量 | |
| D. | 外界条件相同时,放热反应的速率一定大于吸热反应的速率 |
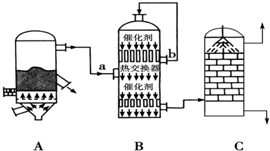
(1)图中设备A的名称是沸腾炉,B设备气流a、b温度较高的是b(填“a”或“b”),C设备中用浓硫酸吸收SO3.
(2)CuFeS2是黄铁矿的另一部分,煅烧时,CuFeS2转化为CuO、Fe2O3和SO2,该反应的化学方程式为:4CuFeS2+13O2$\frac{\underline{\;\;△\;\;}}{\;}$4CuO+2Fe2O3+8SO2.
Ⅱ为了回收利用SO2,研究人员研制了利用低品位软锰矿浆(主要成分是MnO2)吸收高温焙烧含硫废渣产生的SO2废气,制备硫酸锰晶体的生产流程,其流程示意图如下:
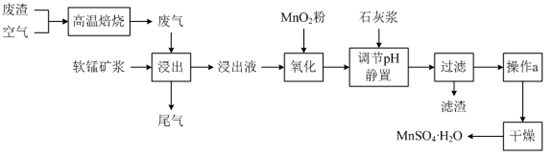
已知,浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+等其他金属离子.有关金属离子形成氢氧化物沉淀时的pH见下表:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 7.6 | 9.7 |
| Fe3+ | 2.7 | 3.7 |
| Al3+ | 3.8 | 4.7 |
| Mn2+ | 8.3 | 9.8 |
(1)写出浸出过程中主要反应的化学方程式:SO2+MnO2=MnSO4.
(2)写出氧化过程中主要反应的离子方程式:2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O.
(3)在氧化后的液体中加入石灰浆,并用pH试纸测定调节pH,pH应调节范围是4.7≤pH<8.3.
(4)滤渣的主要成分有氢氧化铁、氢氧化铝、硫酸钙.
(5)下列各组试剂中,能准确测定尾气中SO2含量的是b、c.(填编号)
a.NaOH溶液、酚酞试液b.稀H2SO4酸化的KMnO4溶液
c.碘水、淀粉溶液d.氨水、酚酞试液.
(1)提出问题:Fe3+、Br2哪一个的氧化性更强?
(2)猜想
①甲同学认为氧化性:Fe3+>Br2,故上述实验现象不是发生化学反应所致,则溶液呈黄色是含Br2(填化学式,下同)所致.
②乙同学认为氧化性:Br2>Fe3+,故上述实验现象是发生化学反应所致,则溶液呈黄色是含Fe3+所致.
(3)设计实验并验证
丙同学为验证乙同学的观点,选用下列某些试剂设计出两种方案进行实验,并通过观察实验现象,证明了乙同学的观点确实是正确的.供选用的试剂:
a.酚酞试液 b.CCl4 c.无水酒精 d.KSCN溶液
请你在下列表格中写出丙同学选用的试剂及实验中观察到的现象.(试剂填序号)
| 选用试剂 | 实验现象 | |
| 方案1 | b | 下层(CCl4层)无色 |
| 方案2 | d | 溶液变为血红色 |
①在足量的稀氯化亚铁溶液中加入l~2滴溴水,溶液呈黄色,所发生的离子反应方程式为2Fe2++Br2═2Fe3++2Br-.
②在FeBr2溶液中通入足量 Cl2,所发生的离子反应方程式为4Fe2++2Br-+3Cl2═4Fe3++Br2+6Cl-.
| A. | NaHS在水中的电离方程式为NaHS═Na++H++S2- | |
| B. | NaHS溶液水解的离子方程式为HS-+H2O═H2S↑+OH- | |
| C. | NaHS溶液与FeSO4溶液反应的离子方程式为S2-+Fe2+═FeS↓ | |
| D. | 向NaHS溶液中滴加过量的新制氯水:HS-+Cl2═S↓+H++2Cl- |
| A. | 1mol/L Na2SO4溶液200mL | B. | 0.9mol/L Na3PO4溶液200mL | ||
| C. | 2.5mol/L NaOH 溶液100mL | D. | 1mol/L NaHCO3溶液300mL |
| A. | 淀粉和纤维素分子式均为(C6H10O5)n,它们水解的最终产物都是葡萄糖,因此淀粉和纤维素互为同分异构体 | |
| B. | 通过蒸馏法、电渗析法、离子交换法等可以实现海水的淡化 | |
| C. | 多糖、蛋白质、油脂均能水解,它们属于天然高分子化合物 | |
| D. | 石油的分馏、煤的干馏、煤的气化和液化均属于物理变化 |
