题目内容
【题目】一定条件下,向密闭恒容容器中加入1.0mol/L X,发生反应:2X(g)Y(g)+Z(g),△H<0,反应到8min时达到平衡;在14min时改变的温度,16min时建立新平衡.X的物质的量浓度变化如图所示.下列有关说法正确的是( ) 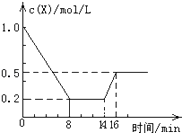
A.0~8min用Y表示的该反应的速度为0.1mol/Lmin
B.8min时达到平衡,该反应的平衡常数为 K=0.5
C.14min时,改变的反应条件是降低了体系的温度
D.16min时的正反应速率,比8min时的正反应速率大
【答案】D
【解析】解:A.由图可知,0~8min内X的浓度变化量为1mol/L﹣0.2mol/L=0.8mol/L,故v(X)= ![]() =0.1mol/(Lmin),根据速率之比等于化学计量数之比,则v(Y)=
=0.1mol/(Lmin),根据速率之比等于化学计量数之比,则v(Y)= ![]() v(X)=
v(X)= ![]() ×0.1mol/(Lmin)=0.05mol/(Lmin),故A错误;
×0.1mol/(Lmin)=0.05mol/(Lmin),故A错误;
B.由图可知,0~8min内X的浓度变化量为1mol/L﹣0.2mol/L=0.8mol/L,则:
2X(g) | Y(g)+ | Z(g) | ||
开始(mol/L) | 1 | 0 | 0 | |
变化(mol/L) | 0.8 | 0.4 | 0.4 | |
平衡(mol/L) | 0.2 | 0.4 | 0.4 |
故该温度下平衡常数k= ![]() =4,故B错误;
=4,故B错误;
C.由图可知,14min时瞬间X的浓度不变,不可能为改变压强,改变条件X的浓度增大,该反应正反应是放热反应,可能为升高温度或增大生成物的物质的量,故C错误;
D.由C分析可知,14min时改变条件为升高温度或增大生成物的物质的量,反应速率加快,故16min平衡时正、逆速率都高于8min时,故D正确;
故选D.
【考点精析】认真审题,首先需要了解化学平衡的计算(反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%).