��Ŀ����
����Ŀ����ͼ��ʾ�ķ�Ӧ��ϵ�У����ֲ��ﱻ��ȥ����֪2 mol��ɫ�����ĩX���ȷֽ⣬�ָ����������ɰ�ɫ����A����ɫҺ��B����ɫ����C��1 mol��X��E��G����ɫ��Ӧ��Ϊ��ɫ��

�ش��������⣺
��1��д���������ʵĻ�ѧʽ��G_____________ D_____________
��2��д��G��C��Ӧ����D�Ļ�ѧ��Ӧ����ʽ��____________________________
��3��д��X��E��A�����ӷ���ʽ��______________________________________
��4��д��C��Na2O2��Ӧ�Ļ�ѧ����ʽ��_____________________________������0.2 mol Na2O2�μӷ�Ӧ��ת�Ƶĵ�����ĿΪ_____________________
���𰸡� NaAlO2 Al(OH)3 NaAlO2 �� CO2 �� 2H2O === Al(OH)3�� �� NaHCO3��2NaAlO2 �� CO2 �� 3H2O === 2Al(OH)3�� �� Na2CO3 HCO![]() �� OH�� === CO
�� OH�� === CO![]() �� H2O 2CO2 �� 2Na2O2 === 2Na2CO3 �� O2 0.2 NA �� 1.204��1023
�� H2O 2CO2 �� 2Na2O2 === 2Na2CO3 �� O2 0.2 NA �� 1.204��1023
��������������������⿼�����ƶϣ���ѧ����ʽ�����ӷ���ʽ����д��������ԭ��Ӧ��ת�Ƶ������ļ�����BΪ��ɫҺ�壬B��Na2O2��Ӧ���ɵ�E����Al��Ӧ����E��G����ɫΪ��ɫ���Ƴ�BΪH2O��EΪNaOH��GΪNaAlO2��C����ɫ���壬C����Na2O2��Ӧ����A��A+HCl��C����AΪNa2CO3��CΪCO2��2 mol��ɫ�����ĩX���ȷֽ⣬�ָ�����������A��B��C��1 mol��X����ɫ��Ӧ�ʻ�ɫ��XΪNaHCO3��C��G��Ӧ����D��CO2��NaAlO2��Һ��Ӧ���ɵ�DΪAl��OH��3��
��1����������������G�Ļ�ѧʽΪNaAlO2��D�Ļ�ѧʽΪAl��OH��3��
��2��G+C��D��CO2��NaAlO2��Һ�ķ�Ӧ����CO2��������Ӧ�Ļ�ѧ����ʽΪNaAlO2+CO2+2H2O=Al��OH��3��+NaHCO3����CO2��������Ӧ�Ļ�ѧ����ʽΪ2NaAlO2+CO2+3H2O=2Al(OH)3��+Na2CO3��
��3��X+E��A��Ӧ�Ļ�ѧ����ʽΪNaHCO3+NaOH=Na2CO3+H2O����Ӧ�����ӷ���ʽΪHCO3-+OH-=CO32-+H2O��
��4��C��Na2O2��Ӧ�Ļ�ѧ����ʽΪ2Na2O2+2CO2=2Na2CO3+O2����˫���ű������ת�Ʒ������ĿΪ��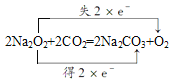 ��2molNa2O2�μӷ�Ӧת��2mol��������0.2molNa2O2�μӷ�Ӧת��0.2mol������ת�Ƶ�����Ϊ0.2NA��1.204
��2molNa2O2�μӷ�Ӧת��2mol��������0.2molNa2O2�μӷ�Ӧת��0.2mol������ת�Ƶ�����Ϊ0.2NA��1.204![]() 1023��
1023��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
