��Ŀ����
����Ŀ��
���ڷ��ֵ�һ����Ȼ��ʮ����������������Al��Cu��Fe���ֽ���Ԫ����ɡ��ش��������⣺
��1������һ����ƽ�����������ϸ�����λ����Ķ��ؾ��壬��ͨ��_______________�������־��塢����ͷǾ��塣
��2����̬Feԭ����_________��δ�ɶԵ��ӣ�Fe3+�ĵ����Ų�ʽΪ_______________���������軯�ؼ���Fe3+���γɵ���������ɫΪ_______________��
��3�����Ƶ�Cu(OH)2�ɽ���ȩ��CH3CHO�����������ᣬ��������ԭ��Cu2O����ȩ��̼ԭ�ӵ��ӻ��������Ϊ____________����ȩ�����и�Ԫ�صĵ縺���ɴ�С��˳��Ϊ_______________������ķе����Ը�����ȩ������Ҫԭ����_____________________________��Cu2OΪ�뵼����ϣ��������������ڲ���4����ԭ�ӣ�������ԭ��λ�����ĺͶ��㣬��þ�������___________��ͭԭ�ӡ�
��4��Al����Ϊ�����������壬�侧������a��0.405nm����������ԭ�ӵ���λ��Ϊ__________����ʽ��ʾAl���ʵ��ܶ�_______________ g��cm-3��
���𰸡� X �������䷨ 4 1s22s22p63s23p63d5 ��[Ar] 3d5 Ѫ��ɫ sp3��sp2 O��C��H �����γ��˷��Ӽ���������ɷе����� 16 12 ![]()
��������(1)��������������ߣ�����X������ӷ��֣������X���߷������䣬�Ǿ��岻�������䣬������ڶ���֮�䣬���ͨ��������������ȷ�����ʴ�Ϊ��X�������䣻
(2)26��Ԫ��Fe��̬ԭ�Ӻ�������Ų�ʽΪ1s22s22p63s23p63d64s2����֪��3d�ϴ���4��δ�ɶԵ��ӣ�ʧȥ���ӱ�Ϊ������ʱ����ʧȥ4s�ϵ�2�����Ӻ�ʧȥ3d�ϵ�1�����ӣ����Fe3+�ĵ����Ų�ʽΪ1s22s22p63s23p63d5�����軯��ΪѪ��ɫ���ʴ�Ϊ��4��1s22s22p63s23p63d5��Ѫ��ɫ��
(3)��ȩ�м��ϵ�C�γ�4���Ҽ����µ��Ӷԣ���˲�ȡsp3�ӻ����ͣ�ȩ���е�C�γ�3���Ҽ���1���м����µ��Ӷԣ���ȡsp2�ӻ����ͣ�Ԫ�صķǽ�����Խǿ���縺����ֵԽ����ȩ�����и�Ԫ�صĵ縺���ɴ�С��˳��ΪO��C��H��������Ӽ���γ��������ȩ�����γ��������������ķе������ȩ���ʴ�Ϊ��sp3��sp2��O��C��H��������ڷ��Ӽ��������ɷе����ߣ�
(4)�þ�����Oԭ����Ϊ4��1+6��![]() +8��
+8��![]() =8����Cu2O��Cu��O�ı�����֪�þ�����ͭԭ����ΪOԭ������2������Ϊ16������Al�����һ��������������������������Alԭ����ͨ�������������������ϣ�����ռ
=8����Cu2O��Cu��O�ı�����֪�þ�����ͭԭ����ΪOԭ������2������Ϊ16������Al�����һ��������������������������Alԭ����ͨ�������������������ϣ�����ռ![]() ��ͨ��һ��������γ�8����������˸þ�������ԭ�ӵ���λ��Ϊ8��3��
��ͨ��һ��������γ�8����������˸þ�������ԭ�ӵ���λ��Ϊ8��3��![]() =12��һ��������Alԭ����Ϊ8��
=12��һ��������Alԭ����Ϊ8��![]() +6��
+6��![]() =4�����Al���ܶȦ�=
=4�����Al���ܶȦ�=![]() =
=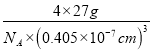 =
=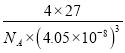 gcm-3���ʴ�Ϊ��16��12��
gcm-3���ʴ�Ϊ��16��12�� 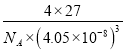 ��
��

 ����ͼ���������������ϵ�д�
����ͼ���������������ϵ�д�

