题目内容
15.重晶石矿的主要成分为硫酸钡,纯净的硫酸钡才能供医用作“钡餐”.硫化钡是可溶于水的盐.讨论用重晶石矿制硫酸钡,设计流程如下: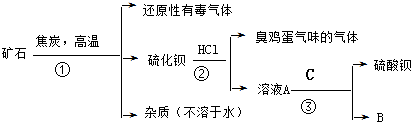
(1)写出步骤①的化学反应方程式BaSO4+4C$\frac{\underline{\;高温\;}}{\;}$BaS+4CO↑,该反应产生的气体具有作燃料、冶炼金属等用途.为进行反应②先要分离出硫化钡,采用的方法是溶解过滤.反应前要在溶液中滴入少量Ba(OH)2溶液,其作用是:防止BaS发生水解.
(2)若B物质在该生产过程中可循环使用,则反应③的化学方程式是:BaCl2+H2SO4=BaSO4↓+2HCl.
(3)有人提出反应②产生了有臭鸡蛋气味的有毒气体,可采用改变反应物的方法避免产生该气体,则反应②的化学方程式是:BaS+CuCl2=CuS↓+BaCl2.此时若要B物质还能循环使用,则C为CuSO4 (写化学式).BaSO4是因为具有既不溶于水也不溶于一般酸、不能被X射线透过等性质而可用作“钡餐”.
分析 (1)重晶石矿的主要成分为硫酸钡,在高温时与焦炭反应生成硫化钡和有毒气体为CO,根据元素守恒写化学方程式;硫化钡是可溶于水的盐,所以通过溶解过滤除去杂质,得硫化钡溶液,硫化钡水解呈碱性,加入碱可抑制其水解;
(2)硫化钡与盐酸反应生成A为氯化钡和硫化氢,溶液A与C反应生成B和硫酸钡,B可循环利用,则B为HCl,C为硫酸,据此写化学方程式;
(3)硫化钡转化成氯化钡可以与盐酸反应也可以与氯化铜反应生成硫化铜沉淀,可以避免产生硫化氢气体,若要B以物质还能循环使用,则C可以用硫酸铜,硫酸铜与氯化钡反应生成氯化铜循环使用,钡离子是重金属离子,钡餐不能溶于水,且要不能被X射线透过,据此答题.
解答 解:(1)重晶石矿的主要成分为硫酸钡,在高温时与焦炭反应生成硫化钡和有毒气体为CO,反应的化学方程式为BaSO4+4C$\frac{\underline{\;高温\;}}{\;}$BaS+4CO↑,CO可作燃料、冶炼金属,硫化钡是可溶于水的盐,所以通过溶解过滤除去杂质,得硫化钡溶液,硫化钡水解呈碱性,加入Ba(OH)2溶液可抑制其水解,
故答案为:BaSO4+4C$\frac{\underline{\;高温\;}}{\;}$BaS+4CO↑;作燃料;冶炼金属;溶解过滤;防止BaS发生水解;
(2)硫化钡与盐酸反应生成A为氯化钡和硫化氢,溶液A与C反应生成B和硫酸钡,B可循环利用,则B为HCl,C为硫酸,反应③的化学方程式为BaCl2+H2SO4=BaSO4↓+2HCl,
故答案为:BaCl2+H2SO4=BaSO4↓+2HCl;
(3)硫化钡转化成氯化钡可以与盐酸反应也可以与氯化铜反应生成硫化铜沉淀,可以避免产生硫化氢气体,反应②的化学方程式为BaS+CuCl2=CuS↓+BaCl2,若要B以物质还能循环使用,则C可以用硫酸铜,硫酸铜与氯化钡反应生成氯化铜循环使用,钡离子是重金属离子,钡餐不能溶于水,且要不能被X射线透过,
故答案为:BaS+CuCl2=CuS↓+BaCl2;CuSO4;既不溶于水也不溶于一般酸;不能被X射线透过.
点评 本题主要考查硫酸钡的提纯,侧重于工业流程的分析与推理,答题时注意元素化合物知识的灵活运用及实验基本操作的应用,题目难度中等,综合性较强.

| A. | 铜与盐酸反应:Cu+2H+═Cu2++H2↑ | |
| B. | 硫酸与氯化钡溶液反应:Ba2++SO42-═BaSO4↓ | |
| C. | 金属钠与水反应:2Na+2H+═2Na++H2↑ | |
| D. | 氯化亚铁与氯水反应:Fe2++Cl2═Fe3++2Cl- |
| A. | 煤 | B. | 氢气 | C. | 石油 | D. | 天然气 |
 K3[Fe(C2O4)3]•3H2O[三草酸合铁(Ⅲ)酸钾晶体]易溶于水,难溶于乙醇,可作为有机反应的催化剂.实验室可用废铁屑等物质为原料制备,并测定产品的纯度.相关反应的化学方程式为:
K3[Fe(C2O4)3]•3H2O[三草酸合铁(Ⅲ)酸钾晶体]易溶于水,难溶于乙醇,可作为有机反应的催化剂.实验室可用废铁屑等物质为原料制备,并测定产品的纯度.相关反应的化学方程式为: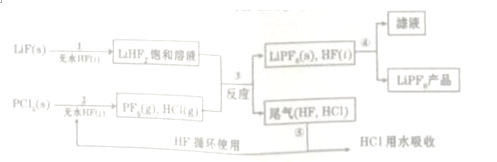
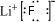 ,无水HF的作用是反应物和溶剂
,无水HF的作用是反应物和溶剂