题目内容
下列说法正确的是( )
| A、可以用稀硝酸和BaCl2溶液检验Na2SO3是否变质 |
| B、可以用碳酸钠溶液除去CO2中的SO2 |
| C、可以用NaOH溶液区别NH4Cl、Al2(SO4)3、CuSO4、FeCl3区别开 |
| D、某溶液中加入BaCl2溶液变浑浊,则此溶液中一定含有CO32? |
考点:物质的检验和鉴别的基本方法选择及应用,物质的分离、提纯的基本方法选择与应用
专题:实验评价题
分析:A.稀硝酸与Na2SO3发生氧化还原反应;
B.CO2和SO2都与碳酸钠溶液反应;
C.加入氢氧化钠,反应的现象各不相同时,可鉴别;
D.加入BaCl2溶液变浑浊,生成的沉淀可能为硫酸钡、碳酸钡或氯化银等.
B.CO2和SO2都与碳酸钠溶液反应;
C.加入氢氧化钠,反应的现象各不相同时,可鉴别;
D.加入BaCl2溶液变浑浊,生成的沉淀可能为硫酸钡、碳酸钡或氯化银等.
解答:
解:A.稀硝酸与Na2SO3发生氧化还原反应,不能鉴别,应先加入盐酸酸化,然后在加入氯化钡溶液检验,如有沉淀生成,说明变质,故A错误;
B.CO2和SO2都与碳酸钠溶液反应,应用饱和碳酸氢钠溶液除杂,故B错误;
C.加入氢氧化钠,NH4Cl有刺激性气体生成,Al2(SO4)3先生成白色沉淀,氢氧化钠过量时沉淀溶解,CuSO4生成蓝色沉淀,FeCl3生成红褐色沉淀,可鉴别,故C正确;
D.加入BaCl2溶液变浑浊,生成的沉淀可能为硫酸钡、碳酸钡或氯化银等,故D错误.
故选C.
B.CO2和SO2都与碳酸钠溶液反应,应用饱和碳酸氢钠溶液除杂,故B错误;
C.加入氢氧化钠,NH4Cl有刺激性气体生成,Al2(SO4)3先生成白色沉淀,氢氧化钠过量时沉淀溶解,CuSO4生成蓝色沉淀,FeCl3生成红褐色沉淀,可鉴别,故C正确;
D.加入BaCl2溶液变浑浊,生成的沉淀可能为硫酸钡、碳酸钡或氯化银等,故D错误.
故选C.
点评:本题考查较为综合,涉及物质的分离、检验和鉴别,为高考常见题型和高频考点,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质的异同以及实验的严密性和可行性的评价,难度中等.

练习册系列答案
 全程金卷系列答案
全程金卷系列答案 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3=K2O+5Na2O+16N2↑,对于该反应,下列判断正确的是( )
| A、NaN3中氮元素的化合价为-3 |
| B、氧化剂和还原剂是同一物质 |
| C、反应过程中若转移1mol电子,则产生2.24L气体(标准状况) |
| D、被氧化的氮原子与生成的氮气分子个数之比为15:8 |
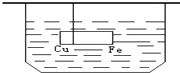 在装有水的容器中,用棉线悬挂一个在水中保持平衡的金属棒,该棒由铁和铜焊接而成,棉线系在两种金属接缝处(如图),再向水中加入少量CuSO4,经过一段时间应看到的现象是( )
在装有水的容器中,用棉线悬挂一个在水中保持平衡的金属棒,该棒由铁和铜焊接而成,棉线系在两种金属接缝处(如图),再向水中加入少量CuSO4,经过一段时间应看到的现象是( )| A、铁端将附着铜增重下沉 |
| B、铜端将附着铜增重下沉 |
| C、铁端将变细减重上升 |
| D、铜端粗细不变将下沉 |
设NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A、在密闭容器中,使1mol N2与3mol H2充分反应后生成NH3的分子数为2NA |
| B、标准状况下,4.48L N2中含有的共用电子对数为0.2NA |
| C、常温常压下,1mol NaHSO4晶体中含有的离子总数为2NA |
| D、标准状况下,1mol Fe与2.24L Cl2完全反应后转移的电子数为3NA |
类推是一种重要的学习方法,但如果不具体问题具体分析就会得出错误结论.下列类推结论正确的是( )
| A、SiH4的熔沸点比CH4高,则PH3的熔沸点比NH3高 |
| B、钠在空气中燃烧生成过氧化钠,则锂在空气中燃烧生成过氧化锂 |
| C、Al(OH)3能溶于NaOH溶液,则Be(OH)2能溶于NaOH溶液 |
| D、甲酸甲酯能发生银镜反应,则乙酸甲酯能发生银镜反应 |
设NA为阿伏加德罗常数值,下列叙述中不正确的是( )
| A、12.4g白磷晶体中含有的P-P键数是0.6NA |
| B、2.9g熟石膏2CaSO4?H2O 含有的结晶水分子数为0.02NA |
| C、100g的98%的浓 H2SO4中所含的硫原子数为NA |
| D、2mol SO2和1mol O2混合在一定条件下密闭容器中加热反应后,容器内物质分子数大于2NA |
NA表示阿伏加德罗常数,下列说法正确的是( )
| A、常温常压下,6g二氧化硅含有Si-O键数目为2NA |
| B、54克Al与氢氧化钠反应产生气体67.2L |
| C、Na与足量O2反应生成1mol Na2O或1mol Na2O2均失去2NA电子 |
| D、各5.6g铁分别与足量的盐酸反应,电子转移总数均为0.3NA |
下列说法正确的是( )
| A、Al与S直接化合可以得到Al2S3,Fe与S直接化合也可以得到Fe2S3 |
| B、水银、水玻璃、胆矾都是纯净物 |
| C、HCl、NH3、BaSO4都是电解质 |
| D、丁达尔现象可以用来区别胶体和溶液 |