题目内容
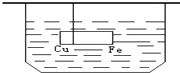 在装有水的容器中,用棉线悬挂一个在水中保持平衡的金属棒,该棒由铁和铜焊接而成,棉线系在两种金属接缝处(如图),再向水中加入少量CuSO4,经过一段时间应看到的现象是( )
在装有水的容器中,用棉线悬挂一个在水中保持平衡的金属棒,该棒由铁和铜焊接而成,棉线系在两种金属接缝处(如图),再向水中加入少量CuSO4,经过一段时间应看到的现象是( )| A、铁端将附着铜增重下沉 |
| B、铜端将附着铜增重下沉 |
| C、铁端将变细减重上升 |
| D、铜端粗细不变将下沉 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:铁和铜连接浸入硫酸铜溶液中,该装置构成了原电池,较活泼的金属作负极,较不活泼的金属作正极,根据正负极上发生的电极反应判断反应现象.
解答:
解:铁和铜连接浸入硫酸铜溶液中,该装置构成了原电池,较活泼的金属作负极,较不活泼的金属作正极,
则负极上铁失电子生成亚铁离子进入溶液,所以铁圈质量减少;
铜上铜离子得电子生成铜单质附着在铜端,导致铜质量增加,所以观察到的现象是:铜增重下沉.
故选BC.
则负极上铁失电子生成亚铁离子进入溶液,所以铁圈质量减少;
铜上铜离子得电子生成铜单质附着在铜端,导致铜质量增加,所以观察到的现象是:铜增重下沉.
故选BC.
点评:本题考查原电池知识,是中等难度的试题,试题基础性强,注重答题的灵活性,有利于巩固基础,提高能力,也有利于培养学生的逻辑推理能力和发散思维能力.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
由短周期元素构成的某离子化合物中,一个阳离子和一个阴离子核外电子数之和为20.下列说法中正确的是( )
| A、化合物中阳离子和阴离子的个数不一定相等 |
| B、化合物中一定只有离子键没有共价键 |
| C、所含元素一定不在同一周期也不在第一周期 |
| D、化合物中阳离子半径一定大于阴离子半径 |
下列说法不正确的是( )
| A、副族元素次外层的d能级上的电子数均未达到10个 |
| B、短周期元素的内层电子均达到了饱和 |
| C、主族元素的次外层电子数为2个或8个或18个 |
| D、第三周期元素的次外层电子均为8个 |
碱性电池具有容量大、放电电流大的特点,因而得到广泛使用,锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应为Zn+2MnO2+H2O═Zn(OH)2+Mn2O3,下列说法错误的是( )
| A、电池工作时,锌失去电子 |
| B、电池正极反应式为:2MnO2+H2O+2e-═Mn2O3+2OH- |
| C、电池工作时,负极附近pH降低 |
| D、正极是水电离出的H+得到电子 |
下列说法正确的是( )
| A、可以用稀硝酸和BaCl2溶液检验Na2SO3是否变质 |
| B、可以用碳酸钠溶液除去CO2中的SO2 |
| C、可以用NaOH溶液区别NH4Cl、Al2(SO4)3、CuSO4、FeCl3区别开 |
| D、某溶液中加入BaCl2溶液变浑浊,则此溶液中一定含有CO32? |
现有Fe、CuO、CuCl2、Ca(OH)2、稀H2SO4等五种物质,在常温下它们两两相互发生的化学反应有( )
| A、7个 | B、6个 | C、4个 | D、5个 |
下列关于浓HNO3与浓H2SO4的叙述正确的是( )
| A、常温下都可用铁制容器贮存 |
| B、常温下都能与铜较快反应 |
| C、露置于空气中,溶液质量均减轻 |
| D、露置于空气中,溶液浓度均升高 |
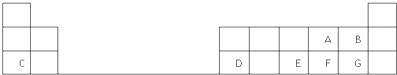
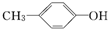 ;③
;③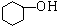 ;④CH3CH2Cl;⑤CCl4;⑥CH≡CH;⑦
;④CH3CH2Cl;⑤CCl4;⑥CH≡CH;⑦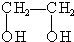 ; ⑧CH3CH2OH.
; ⑧CH3CH2OH.