题目内容
汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3=K2O+5Na2O+16N2↑,对于该反应,下列判断正确的是( )
| A、NaN3中氮元素的化合价为-3 |
| B、氧化剂和还原剂是同一物质 |
| C、反应过程中若转移1mol电子,则产生2.24L气体(标准状况) |
| D、被氧化的氮原子与生成的氮气分子个数之比为15:8 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:该反应中叠氮化钠中N元素化合价由-
价变为0价、硝酸钾中N元素化合价由+5价变为0价,所以硝酸钾是氧化剂、叠氮化钠是还原剂,再结合方程式分析解答.
| 1 |
| 3 |
解答:
解:A.叠氮化钠中N元素化合价由-
价变为0价,故A错误;
B.硝酸钾是氧化剂、叠氮化钠是还原剂,故B错误;
C.反应过程中若转移1mol电子,则参加反应的叠氮酸钠的物质的量为1mol,生成氮气的物质的量=
×16=1.6mol,则产生35.84L气体(标准状况),故C错误;
D.被氧化的氮原子与生成的氮气分子个数之比为30:16=15:8,故D正确;
故选D.
| 1 |
| 3 |
B.硝酸钾是氧化剂、叠氮化钠是还原剂,故B错误;
C.反应过程中若转移1mol电子,则参加反应的叠氮酸钠的物质的量为1mol,生成氮气的物质的量=
| 1mol |
| 10 |
D.被氧化的氮原子与生成的氮气分子个数之比为30:16=15:8,故D正确;
故选D.
点评:本题考查了氧化还原反应,明确方程式中元素化合价变化是解本题关键,注意叠氮化钠中氮元素化合价,为易错点.

练习册系列答案
相关题目
下列化合物的沸点由高到低的顺序正确的是( )
①CH3CH2CH2CH2Cl ②CH3CH2CH2CH2Br ③CH3CH(CH3)CH2Cl ④CH3CH2CH2CH3.
①CH3CH2CH2CH2Cl ②CH3CH2CH2CH2Br ③CH3CH(CH3)CH2Cl ④CH3CH2CH2CH3.
| A、②①④③ | B、②④①③ |
| C、②①③④ | D、①③②④ |
由短周期元素构成的某离子化合物中,一个阳离子和一个阴离子核外电子数之和为20.下列说法中正确的是( )
| A、化合物中阳离子和阴离子的个数不一定相等 |
| B、化合物中一定只有离子键没有共价键 |
| C、所含元素一定不在同一周期也不在第一周期 |
| D、化合物中阳离子半径一定大于阴离子半径 |
下列烷烃的一氯取代物中没有同分异构体的是( )
①丙烷 ②丁烷 ③异丁烷 ④新戊烷.
①丙烷 ②丁烷 ③异丁烷 ④新戊烷.
| A、有4种 | B、有3种 |
| C、有2种 | D、只有1种 |
下列说法不正确的是( )
| A、副族元素次外层的d能级上的电子数均未达到10个 |
| B、短周期元素的内层电子均达到了饱和 |
| C、主族元素的次外层电子数为2个或8个或18个 |
| D、第三周期元素的次外层电子均为8个 |
下列说法正确的是( )
| A、可以用稀硝酸和BaCl2溶液检验Na2SO3是否变质 |
| B、可以用碳酸钠溶液除去CO2中的SO2 |
| C、可以用NaOH溶液区别NH4Cl、Al2(SO4)3、CuSO4、FeCl3区别开 |
| D、某溶液中加入BaCl2溶液变浑浊,则此溶液中一定含有CO32? |
甲烷在一定条件下可生成下列四种微粒,其中,键角为120°的是( )
| A、碳正离子(CH3+) |
| B、碳负离子(CH3-) |
| C、甲基(-CH3) |
| D、碳烯(:CH2) |
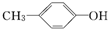 ;③
;③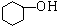 ;④CH3CH2Cl;⑤CCl4;⑥CH≡CH;⑦
;④CH3CH2Cl;⑤CCl4;⑥CH≡CH;⑦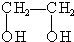 ; ⑧CH3CH2OH.
; ⑧CH3CH2OH.