题目内容
【题目】煤炭燃烧过程中会释放出大量的SO2,严重破坏生态环境。采用一定的脱硫技术可以把硫元素以CaSO4的形式固定,从而降低SO2的排放。但是煤炭燃烧过程中产生的CO又会与CaSO4发生化学反应,降低脱硫效率。相关反应的热化学方程式如下:
CaSO4(s)+CO(g) ![]() CaO(s)+SO2(g)+CO2(g) ΔH1=+218.4kJ·mol-1(反应Ⅰ)
CaO(s)+SO2(g)+CO2(g) ΔH1=+218.4kJ·mol-1(反应Ⅰ)
CaSO4(s)+4CO(g) ![]() CaS(s)+4CO2(g) ΔH2= -175.6kJ·mol-1(反应Ⅱ)
CaS(s)+4CO2(g) ΔH2= -175.6kJ·mol-1(反应Ⅱ)
请回答下列问题:
(1)假设某温度下,反应Ⅰ的速率(v1)大于反应Ⅱ的速率(v2),则下列反应过程能量变化示意图正确的是__________。
A. 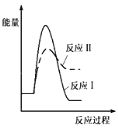 B.
B. 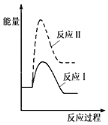
C. 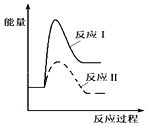 D.
D.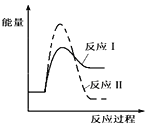
(2)在温度、容积相同且不变的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下表(已知2SO2(g)+O2(g) ![]() 2SO3(g)△H=196.6kJ·mol-1) 则:
2SO3(g)△H=196.6kJ·mol-1) 则:
容器 | 甲 | 乙 | 丙 | (填>,=,<) A.2c1_____c3 B.a+b_____196.6 C.2p2____p3 D.α1+α3___1 |
反应物投入量 | 2mol SO2、1mol O2 | 2mol SO3 | 4mol SO3 | |
SO3的浓度 (mol·L-1) | C1 | C2 | C3 | |
反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ | |
体系压强 | P1 | P2 | P3 | |
反应物转化率 | α1 | α2 | α3 |
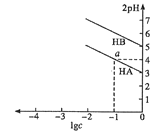
(3)“亚硫酸盐法”吸收烟气中的SO2。室温条件下,将烟气通入氨水中,测得溶液pH与含硫组分物质的量分数的变化关系如图所示。

请写出a点时n(HSO3-):n(H2SO3)=______,b点时溶液pH=7,则n(NH4+):n(HSO3-)=_____。
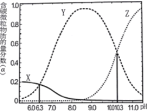
(4)催化氧化法去除NO,一定条件下,用NH3消除NO污染,其反应原理为4NH3+6NO ![]() 5N2+ 6H2O。不同温度条件下,n(NH3):n(NO)的物质的量之比分别为4:l、3:l、1:3时,得到NO脱除率曲线如图所示:
5N2+ 6H2O。不同温度条件下,n(NH3):n(NO)的物质的量之比分别为4:l、3:l、1:3时,得到NO脱除率曲线如图所示:
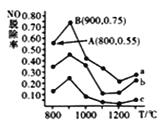
①曲线c对应NH3与NO的物质的量之比是__________。
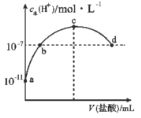
②曲线a中NO的起始浓度为6×10-4mg/m3,从A点到B点经过0.8s,该时间段内NO的脱除速率为__________mg/(m3·s)。
(5)已知Ksp(BaSO4)=1×10-10,Ksp(BaCO3)=2.5×10-9,向0.4mol/L Na2SO4的溶液中加入足量BaCO3粉末(忽略体积变化),充分搅拌,发生反应SO42- (aq)+BaCO3(s) ![]() BaSO4 (s)+CO32-(aq) 静置后沉淀转化达到平衡。此时溶液中的c(SO42-)=____mol·L-1(保留小数点后两位).
BaSO4 (s)+CO32-(aq) 静置后沉淀转化达到平衡。此时溶液中的c(SO42-)=____mol·L-1(保留小数点后两位).
【答案】D < = > < 1:1 3:1 1:3 1.5×10-4 0.02
【解析】
(1)反应Ⅰ为吸热反应,生成物物的总能量高于反应物,反应Ⅱ为放热反应,生成物的总能量低于反应物,由反应Ⅰ的速率(v1)大于反应Ⅱ的速率(v2)可知,反应Ⅰ活化能小于反应Ⅱ;
(2)由表格数据可知,甲容器与乙容器是等效平衡,丙容器可以视为在乙的基础上压强增大一倍,平衡向正反应方向移动;
(3)根据图象可知a点时两个比值相等,b点时溶液pH=7,根据电荷守恒可知n(NH4+)=n(HSO3-)+2n(SO32-),又根据图象曲线可知,n(HSO3-)=n(SO32-),则n(NH4+):n(HSO3-)=(1:2):1=3:1;
(4)①由化学平衡移动原理可知,相同温度时,n(NH3):n(NO)的物质的量之比越大,NO脱除率越大;
②由图给数据计算可得;
由反应方程式可知![]() =
=![]() ,由题给数据计算可得。
,由题给数据计算可得。
(1)反应Ⅰ为吸热反应,生成物物的总能量高于反应物,反应Ⅱ为放热反应,生成物的总能量低于反应物,则A、B错误;由反应Ⅰ的速率(v1)大于反应Ⅱ的速率(v2)可知,反应Ⅰ活化能小于反应Ⅱ,则C错误、D正确,故答案为:D;
(2)由表格数据可知,甲容器与乙容器是等效平衡,则浓度c1=c2,转化率α1+α2=1,甲与乙的反应的能量变化之和为196.6kJ,a+b=196.6;丙容器可以视为在乙的基础上压强增大一倍,平衡向正反应方向移动,则丙中三氧化硫的浓度c3>2c2,转化率α3<α2,平衡移动不能消除压强增大,容器中压强p2<p3<2p2,由α1+α2=1和α3<α2可得α1+α3<1,故答案为:<;=;>;<;
(3)根据图象可知a点时两个比值相等,则n(HSO3-):n(H2SO3)=1:1;b点时溶液pH=7,根据电荷守恒可知n(NH4+)=n(HSO3-)+2n(SO32-),又根据图象曲线可知,n(HSO3-)=n(SO32-),则n(NH4+):n(HSO3-)=(1:2):1=3:1,故答案为:1:1;3:1;
(4)①由化学平衡移动原理可知,相同温度时,n(NH3):n(NO)的物质的量之比越大,NO脱除率越大,由图可知,温度相同时,曲线c的NO脱除率最小,则曲线c对应NH3与NO的物质的量之比是1:3,故答案为:1:3;
②曲线a中NO的起始浓度为6×10-4mg/m3,由图可知从A点到B点经过0.8s,该时间段内NO的脱除速率为![]() =1.5×10-4 mg/(m3·s),故答案为:1.5×10-4;
=1.5×10-4 mg/(m3·s),故答案为:1.5×10-4;
(5)设反应后c(SO42-)为xmol/L,则消耗c(SO42-)为(0.4—x)mol/L,反应生成c(CO32-)为(0.4—x)mol/L,由反应方程式可知![]() =
=![]() ,则有
,则有![]() =
=![]() ,解得x≈0.02mol/L,故答案为:0.02.
,解得x≈0.02mol/L,故答案为:0.02.

 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案【题目】已知1L无色待测液中除含有0.2mo/L的Na+外,还可能含下列离子中的一种或几种:
阳离子 | K+、NH4+、Ca2+、Ba2+、Fe3+ |
阴离子 | Cl-、Br-、CO32-、HCO3-、SO42- |
现进行如图实验操作(每次实验所加试剂均过量)
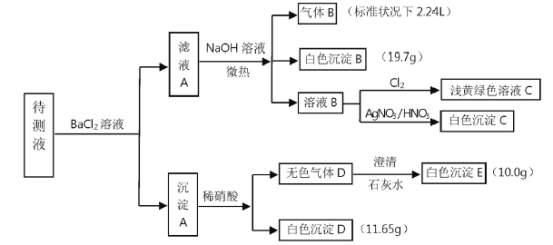
(1)由气体B可确定待测液中含有的离子是___________。
(2)由白色沉淀D和白色沉淀E可以判定待测液中一定含有的离子是___________,据此可以确定待液中一定不存在的离子是___________。
(3)由白色沉淀B可确定待测液中含有的离子是___________。
(4)某同学认为待液中一定不含溴离子,判断的依据是______________________。
(5)综上分析,待测液中K+的最小浓度为___________。