题目内容
【题目】常温下,向1 L pH=10的 NaOH溶液中持续通入CO2。通入CO2的体积(V)与溶液中水电离产生的OH-离子浓度(c)的关系如图所示。
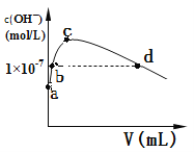
(1)c点溶液中离子浓度由大至小的关系是:________________________________________________。
(2)a点溶液中由水电离产生的c(H+)=______________;b点溶液中c(H+)________1×10-7mol/L(填写“等于”、“大于”或“小于”)。
(3)能使0.1mol/L乙酸溶液的电离程度以及pH都增大的是___。(选填序号)
a.加水稀释 b.加入少量乙酸钠固体 c.通氯化氢 d.加入少量苛性钠固体
【答案】c(Na+)>c(CO32-)>c(OH-)>c(HCO3—)>c(H+) 1×10-10 mol/L 小于 ad
【解析】
二氧化碳通入氢氧化钠,溶液在ab段为氢氧化钠和碳酸钠的混合溶液,抑制水的电离,bc段,氢氧化钠不断被消耗;到达c点,溶液为碳酸钠溶液,cd段碳酸钠溶液不断转变为碳酸氢钠溶液。
(1)c点为碳酸钠溶液,溶液显碱性,离子浓度由大至小的关系是:c(Na+)>c(CO32-)>c(OH-)>c(HCO3—)>c(H+);
(2)a点为氢氧化钠溶液,由水电离产生的c(H+)=溶液中的c(H+)=10-pH=1×10-10 mol/L;b点为氢氧化钠和碳酸钠的混合液,溶液显碱性,c(H+)小于1×10-7mol/L;
(3) a.加水稀释,平衡正向移动,电离程度增大,pH值增大;
b.加入少量乙酸钠固体,溶液中醋酸根浓度增大,电离平衡逆向移动,电离程度减小;
c.通氯化氢,溶液中氢离子浓度增大,电离平衡逆向移动,pH减小;
d.加入少量苛性钠固体,溶液中氢离子浓度减小,电离平衡正向移动,pH增大。
综上所述,能使0.1mol/L乙酸溶液的电离程度以及pH都增大的是AD。

【题目】用以下图示装置研究物质的性质,能够获得可靠结论的是
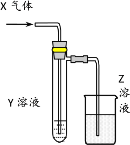
X | Y | Z | 结论 | |
A | HCHO | 新制Cu(OH)2 | NaOH(aq) | 验证甲醛的还原性 |
B | CH3Cl | AgNO3(aq) | NaOH(aq) | 验证一氯甲烷含氯元素 |
C | SO2 | KMnO4(aq) | NaOH(aq) | 验证二氧化硫的漂白性 |
D | Cl2 | 淀粉KI(aq) | NaOH(aq) | 验证氯气的强氧化性 |
A.AB.BC.CD.D