题目内容
18.下列有关元素化合物的叙述中正确的是( )| A. | 钠在空气中燃烧生成白色的氧化钠固体 | |
| B. | 检验FeCl2溶液中的少量Fe3+,可以用KSCN溶液 | |
| C. | 二氧化硫的水溶液能使紫色石蕊溶液变红,随后使之褪色 | |
| D. | 普通玻璃的组成可用Na2O•CaO•6SiO2表示,是纯净物 |
分析 A.钠在空气中燃烧生成淡黄色过氧化钠;
B.铁离子和KSCN溶液混合产生血红色溶液,亚铁离子和KSCN溶液不反应;
C.二氧化硫具有漂白性,但不能漂白酸碱指示剂;
D.普通玻璃的组成可用Na2O•CaO•6SiO2表示,但玻璃中存在硅酸钠、硅酸钙和二氧化硅.
解答 解:A.钠在空气中燃烧生成淡黄色过氧化钠,钠和空气接触生成白色固体氧化钠,故A错误;
B.铁离子和KSCN溶液混合产生血红色溶液,亚铁离子和KSCN溶液不反应,所以可以用KSCN溶液检验铁离子,故B正确;
C.二氧化硫具有漂白性,但不能漂白酸碱指示剂,二氧化硫和水反应生成亚硫酸,亚硫酸电离出氢离子而导致其溶液呈酸性,所以二氧化硫水溶液遇紫色石蕊试液变红色,但不褪色,故C错误;
D.普通玻璃的组成可用Na2O•CaO•6SiO2表示,但玻璃中存在硅酸钠、硅酸钙和二氧化硅,所以玻璃是混合物,故D错误;
故选B.
点评 本题考查钠的性质、铁离子检验、二氧化硫性质、混合物和纯净物判断等知识点,侧重考查元素化合物知识及基本概念,知道铁离子及亚铁离子的检验方法及实验现象,易错选项是C.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.下列事实中不能证明CH3COOH是弱电解质的是( )
| A. | 常温下某CH3COONa溶液的pH=8 | |
| B. | 用CH3COOH溶液做导电实验,灯泡很暗 | |
| C. | 等pH等体积的盐酸、CH3COOH溶液和足量锌反应,CH3COOH放出的氢气较多 | |
| D. | CH3COONa和H3PO4反应,生成CH3COOH. |
6.150℃、1.01×105 Pa时,aL乙炔和aL丙烯的混合气体与过量的bLO2混合、点燃,使这两种烃充分燃烧后,再恢复到原状况,此时混合气体的体积为( )
| A. | 10aL | B. | (2a+b)L | C. | (b-a)L | D. | 无法计算 |
3.下列反应所得溶液中,一定只含一种溶质的是( )
| A. | 向铁粉中加入稀硝酸 | |
| B. | 向烧碱溶液中通入CO2气体 | |
| C. | 向稀盐酸中滴入少量的NaAlO2溶液 | |
| D. | 向MgSO4、H2SO4的混合溶液中加入过量的Ba(OH)2溶液 |
10.下列热化学方程式或离子方程式中,正确的是( )
| A. | 0.01mol•L-1NH4Al(SO4)2溶液与0.02mol•L-1Ba(OH)2溶液等体积混合:NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3•H2O | |
| B. | 一定条件下,将0.5mol N2(g)和1.5molH2(g)置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-38.6kJ•mol-1 | |
| C. | 如图表示H2与O2发生反应过程中的能量变化,H2的燃烧热为571.6 kJ•mol-1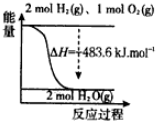 | |
| D. | CO(g)的燃烧热是283.0 kJ•mol-1,则CO2分解的热化学方程式为:2CO2(g)=2CO(g)+O2(g)△H=+283.0 kJ•mol-1 |
7.用惰性电极电解下列溶液时,阴极和阳极上的主要产物分别是H2和O2的是( )
| A. | 酸性AgNO3溶液 | B. | HCl溶液 | C. | 稀NaOH溶液 | D. | 酸性CuSO4溶液 |
8.下列电子式书写正确的是( )
| A. | N2: | B. | NH3 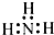 | C. | H2O H+[:O:]2-H+ | D. | NaCl  |
 研究性学习小组进行CH4的性质探究实验.
研究性学习小组进行CH4的性质探究实验. B.
B. C.甲醇 D.CH3-O-CH3E.HO-CH2CH2-OH
C.甲醇 D.CH3-O-CH3E.HO-CH2CH2-OH