题目内容
18.电石是一种遇水即产生可燃性气体的物质,主要成分是CaC2,常含有杂质CaS.①CaC2中所含化学键类型是离子键、非极性共价键阴离子电子式为
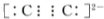
②写出CaC2与盐酸反应的化学方程式CaC2+2HCl═CaCl2+C2H2↑.
分析 ①碳化钙为离子化合物,其化学式中含有钙离子和C22-离子,含有的化学式为离子键和非极性共价键;
C22-中每个C原子最外层平均有5个电子,根据8电子稳定结构可知,C原子之间应形成3对共用电子对,据此写出其电子式;
②碳化钙与水反应生成乙炔和氢氧化钙,氢氧化钙与盐酸反应生成氯化钙和水,据此写出总的化学方程式.
解答 解:①碳化钙中含有钙离子和C22-离子,属于离子化合物,其化学式中含有离子键和非极性共价键;
C22-中每个C原子最外层平均有5个电子,根据8电子稳定结构可知,C原子之间应形成3对共用电子对,C22-的电子式为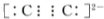 ,
,
故答案为:离子键、非极性共价键;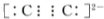 ;
;
②碳化钙与盐酸反应生成氯化钙和乙炔气体,反应的化学方程式为:CaC2+2HCl═CaCl2+C2H2↑;
故答案为:CaC2+2HCl═CaCl2+C2H2↑.
点评 本题考查了化学键与反应方程式的书写,充分考查了学生的分析、理解能力及灵活应用能力,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.在下列反应中,HCl既表现酸性又表现氧化性的是( )
| A. | CaCO3+2HCl=CaCl2+H2O+CO2↑ | |
| B. | Fe+2HCl═FeCl2+H2↑ | |
| C. | MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑ | |
| D. | NaOH+HCl=NaCl+H2O |
9.一定量的CuS和Cu2S的混合物投入足量的HNO3中,收集到气体VL(标准状况),向反应后的溶液中(存在Cu2+和SO42-)加入足量NaOH,产生蓝色沉淀,过滤,洗涤,灼烧,得到CuO12.0g,若上述气体为NO和NO2的混合物,且体积比为1﹕1,则V可能为( )
| A. | 13.5L | B. | 9.0L | C. | 16.8L | D. | 15.7L |
13.在下列物质:A.烧碱 B.硫酸 C.干冰 D.硫酸钡 E.纯碱 F.铁
(1)既不是电解质,也不是非电解质的是F(或铁).
(2)纯碱的电离方程式是Na2CO3=2Na++CO32-.
(3)烧碱溶液与稀硫酸混合,发生反应的离子方程式为H++OH-=H2O.
(4)将干冰升华后所得的气体通入过量烧碱溶液中,发生反应的离子方程式为
CO2+2OH-=CO32-+H2O.
(5)a、b、c、d是Na2CO3、BaCl2、HCl、AgNO3四种溶液中的一种,现将它们两两混合,现象如下表所示:
①b是HCl(用化学式填写).
②写出a+c反应的离子方程式Ag++Cl-=AgCl↓.
盐酸分子式:HCl相对分子质量:36.5密度:1.19g/cm3质量分数:36.5%
(1)既不是电解质,也不是非电解质的是F(或铁).
(2)纯碱的电离方程式是Na2CO3=2Na++CO32-.
(3)烧碱溶液与稀硫酸混合,发生反应的离子方程式为H++OH-=H2O.
(4)将干冰升华后所得的气体通入过量烧碱溶液中,发生反应的离子方程式为
CO2+2OH-=CO32-+H2O.
(5)a、b、c、d是Na2CO3、BaCl2、HCl、AgNO3四种溶液中的一种,现将它们两两混合,现象如下表所示:
| 反应物 | a+b | c+d | a+d | a+c | b+d |
| 现象 | 白色沉淀 | 白色沉淀 | 白色沉淀 | 白色沉淀 | 无色气体 |
②写出a+c反应的离子方程式Ag++Cl-=AgCl↓.
盐酸分子式:HCl相对分子质量:36.5密度:1.19g/cm3质量分数:36.5%
3.以下关于硫及其化合物的说法错误的是( )
| A. | 硫元素在自然界中既有游离态,又有化合态 | |
| B. | 浓硫酸不可用来干燥H2S气体,因其具有强氧化性 | |
| C. | 硫单质与铁反应生成硫化铁 | |
| D. | SO2、SO3都为酸性氧化物,都可与水反应生成相应的酸 |
10.苯乙烯是一种重要的有机化工原料,其结构简式为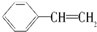 ,它一般不可能具有的性质是( )
,它一般不可能具有的性质是( )
 ,它一般不可能具有的性质是( )
,它一般不可能具有的性质是( )| A. | 易溶于水,不易溶于有机溶剂 | |
| B. | 在空气中燃烧产生浓烟 | |
| C. | 所有的原子可能共平面 | |
| D. | 能与浓硝酸在浓H2SO4作用下发生取代反应 |
8.下列实验操作中错误的是( )
| A. | 称量NaOH时,NaOH置于滤纸上放在托盘天平左盘,砝码放在右盘 | |
| B. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 配制稀硫酸时,先在烧杯中加入一定量水,再沿玻璃棒慢慢加入浓硫酸 |