题目内容
氧化还原反应中实际上包含氧化和还原两个过程,下面是一个还原过程的反应式:NO3-+4H++3e-=NO+2H2O,KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的化学方程式:________________________。
(2)反应中硝酸体现了________、________的性质。
(3)反应中若产生0.2 mol气体,则转移电子的物质的量是________mol。
(4)若1 mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是_________________________________________________________________。
(1)写出并配平该氧化还原反应的化学方程式:________________________。
(2)反应中硝酸体现了________、________的性质。
(3)反应中若产生0.2 mol气体,则转移电子的物质的量是________mol。
(4)若1 mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是_________________________________________________________________。
(1)14HNO3(稀)+3Cu2O=6Cu(NO3)2+2NO↑+7H2O。 (2)酸性 氧化性 (3)0.6(4)使用了较浓的硝酸,产物中有部分二氧化氮生成
(1)从所给还原过程的反应式看NO3-得电子,即HNO3作氧化剂,要能使该反应发生必须加入还原剂,因此甲只能是Cu2O。(3)若产生0.2 mol气体(NO),则转移的电子物质的量为(5-2)×0.2 mol=0.6 mol。(4)若1 mol甲与某浓度硝酸反应时,被还原的硝酸的物质的量增加,根据电子得失守恒推知,可能是使用了较浓的硝酸,使产物中生成了部分NO2。

练习册系列答案
相关题目
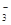 、SO
、SO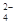 、NH
、NH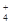 、CO
、CO (不考虑溶液中由水电离的少量的H+和OH-),取200mL该溶液,分为两等份进行下列实验:
(不考虑溶液中由水电离的少量的H+和OH-),取200mL该溶液,分为两等份进行下列实验: