题目内容
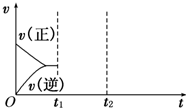
在密闭容器中,反应X2(g)+Y2(g)?2XY(g)△H<0达到甲平衡,在仅改变某一条件后,达到乙平衡,对此条件的分析正确的是( )


| A.图Ⅰ是增大反应物浓度 |
| B.图Ⅱ可能是加入正催化剂 |
| C.图Ⅱ可能是增大压强 |
| D.图Ⅲ是增大压强或升高温度 |
A、增大反应物浓度,正逆反应速率均加快,且正反应速率大于逆反应速率,但是逆反应速率不会摆脱原来的速率变化,故A错误;
B、加入正催化剂,正逆反应速率同等程度的增大,化学平衡不移动,故B正确;
C、反应X2(g)+Y2(g)?2XY(g)为反应前后体积不变的反应,若增大压强,正逆反应速率同等程度的增大,但化学平衡不移动,故C正确;
D、增大压强正逆反应速率同等程度的增大,但化学平衡不移动,由图象可知乙的温度大于甲的温度,升高温度化学平衡逆向移动,XY的含量减小,纵坐标是XY的含量时,才会吻合图象,故D错误.
故选:BC.
B、加入正催化剂,正逆反应速率同等程度的增大,化学平衡不移动,故B正确;
C、反应X2(g)+Y2(g)?2XY(g)为反应前后体积不变的反应,若增大压强,正逆反应速率同等程度的增大,但化学平衡不移动,故C正确;
D、增大压强正逆反应速率同等程度的增大,但化学平衡不移动,由图象可知乙的温度大于甲的温度,升高温度化学平衡逆向移动,XY的含量减小,纵坐标是XY的含量时,才会吻合图象,故D错误.
故选:BC.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目