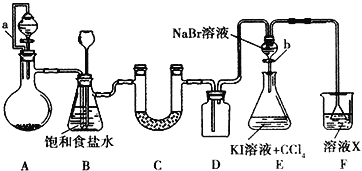
题目内容
【题目】二甲醚(CH3OCH3)和甲醇(CH3OH)被称为21世纪的新型燃料。以CH4和H2O为原料制备二甲醚和甲醇的工业流程如下:
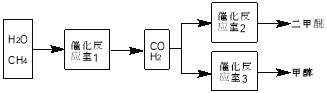
请填空:
(1)在一定条件下,反应室1中发生反应:CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H>0。将1.0molCH4和2.0molH2O通人反应室1(假设容积为100L),10min末有0.1molCO生成,则10min内反应的平均速率V(H2)=________。该反应平衡常数的表达式:_____________。
CO(g)+3H2(g) △H>0。将1.0molCH4和2.0molH2O通人反应室1(假设容积为100L),10min末有0.1molCO生成,则10min内反应的平均速率V(H2)=________。该反应平衡常数的表达式:_____________。
(2)已知:CH3OCH3 (g)+3O2(g)=2CO2(g)+3H2O(g) △H=-1323 KJ/mol;
2H2(g)+O2(g)=2H2O(g) △H=-484 KJ/mol;
CO的燃烧热:283KJ/mol。
在一定条件下,反应室2的可逆反应除生成二甲醚外还生成了气态水,该热化学方程式为_______________。(本题涉及的条件均在同一条件下)
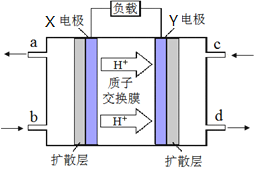
(3) 绿色电源“二甲醚-氧气燃料电池”的工作原理如右图所示,写出X电极的电极反应式_______________
(4)反应室3中在催化剂作用下发生如下反应:CO(g) +2H2(g) ![]() CH3OH(g)。对此反应进行如下研究:
CH3OH(g)。对此反应进行如下研究:
①在容积为1L的密闭容器中分别充入1molCO和2molH2,实验测得甲醇的物质的量和温度、时间的关系曲线如图1所示。
则:该正反应的△H___________0(填“<”、“>”或“=")。
②在容积均为1L的a、b、c三个相同密闭容器中分别充入1mol CO和2mol H2,三个容器的反应温度分别为T1、T2、T3,在其他条件相同情况下,实验测得反应均进行到5min时甲醇的体积分数如图2所示。下列说法正确的是_______________
A.a、b、c三容器5min时的正反应速率大小为:b>a>c
B.达到平衡时,a、b、c三容器中CO转化率为a>b>c
C.5min时,a、b、c三容器中的反应均可能达到平衡状态。
D.将容器b中的平衡状态转变到容器c中的平衡状态,可采取的措施有升温或减压
【答案】(1)0.0003mol·L-1·min-1;K=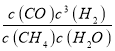 ;
;
(2)2CO(g)+4H2(g)=CH3OCH3(g)+H2O(g) △H=-211 KJ/mol
(3)(CH3)2O-12e-+3H2O=2CO2+12H+;
(4)①<;② BD
【解析】
试题分析:(1)10min末有0.1mol CO生成,根据方程式CH4(g)+H2O(g)CO(g)+3H2(g)可知,生成的氢气为0.1mol×3=0.3mol,容器的体积为100L,则10min内用氢气表示的平均速率v(H2)=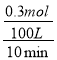 =0.0003mol/(Lmin);该反应平衡常数的表达式为K=
=0.0003mol/(Lmin);该反应平衡常数的表达式为K=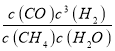 ,故答案为:0.0003 mol/(Lmin);
,故答案为:0.0003 mol/(Lmin);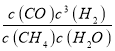 ;
;
(2)已知:①CO的燃烧热为283kJ/mol,则CO(g)+![]() O2(g)═CO2(g)△H=-283kJ/mol;②CH3OCH3(g)+3O2(g)═2CO2(g)+3H2O(g)△H=-1323kJ/mol,③2H2(g)+O2(g)═2H2O(g)△H=-484kJ/mol,利用盖斯定理将①×2+③×2-②可得:2CO(g)+4H2(g)═CH3OCH3(g)+H2O(g)△H= -2×(-283kJ/mol)+2×(-484kJ/mol)-(-1323kJ/mol)= -211kJ/mol,故答案为:2CO(g)+4H2(g)═CH3OCH3(g)+H2O(g)△H=-211kJ/mol;
O2(g)═CO2(g)△H=-283kJ/mol;②CH3OCH3(g)+3O2(g)═2CO2(g)+3H2O(g)△H=-1323kJ/mol,③2H2(g)+O2(g)═2H2O(g)△H=-484kJ/mol,利用盖斯定理将①×2+③×2-②可得:2CO(g)+4H2(g)═CH3OCH3(g)+H2O(g)△H= -2×(-283kJ/mol)+2×(-484kJ/mol)-(-1323kJ/mol)= -211kJ/mol,故答案为:2CO(g)+4H2(g)═CH3OCH3(g)+H2O(g)△H=-211kJ/mol;
(3)根据氢离子移动方向知,左边电极是负极,通入燃料二甲醚,右边电极是正极,通入氧化剂氧气,该燃料电池中,正极上氧气得电子和氢离子反应生成水,电极反应式为O2+4e-+4H+=2H2O;负极的电极反应式为(CH3)2O-12e-+3H2O=2CO2+12H+,故答案为:(CH3)2O-12e-+3H2O=2CO2+12H+;
(4)①从图象可以看出,升高温度,甲醇的物质的量减少,说明正反应是放热反应,则△H<0,故答案为:<,
②A.升高温度,化学反应速率加快,故a、b、C三容器5min时的正反应速率大小为:c>b>a,故A错误;B.该反应为放热反应,升高温度,平衡逆向移动,故达到平衡时,a、b、c中CO转化率为a>b>c,故B正确;C.该反应为放热反应,升高温度,平衡逆向移动,故5min时,a中反应未达平衡,b、c中的反应达到平衡状态,故C错误;D.该反应为放热反应,升高温度,平衡逆向移动;反应后气体体积小于反应前,减小压强.平衡逆向移动,故将容器b中的平衡状态转变到容器c中的平衡状态,可采取的措施有升温或减压,故D正确,故答案为:BD。