题目内容
在298 K、1.01×105 Pa下,将22 g CO2通入750 mL 1 mol·L-1 NaOH溶液中充分反应,测得反应放出x kJ的热量。已知在该条件下,1 mol CO2通入1 L 2 mol·L-1 NaOH溶液中充分反应放出y kJ的热量。则CO2与NaOH溶液反应生成NaHCO3的热化学方程式为( )。
| A.CO2(g)+NaOH(aq)===NaHCO3(aq) ΔH=-(2y-x) kJ·mol-1 |
| B.CO2(g)+NaOH(aq)===NaHCO3(aq) ΔH=-(2x-y) kJ·mol-1 |
| C.CO2(g)+NaOH(aq)===NaHCO3(aq) ΔH=-(4x-y) kJ·mol-1 |
| D.CO2(g)+NaOH(aq)===NaHCO3(aq) ΔH=-(8x-2y) kJ·mol-1 |
C
本题考查化学反应与能量变化。
先算出CO2和NaOH的物质的量,分别是0.5mol和0.75mol.由题意知,CO2过量。首先发生CO2 + 2NaOH="Na2CO3+H2O"
0.375---0.75--
放出热量为0.375y
然后
CO2 + H2O+Na2CO3=2NaHCO3,设反应热为Z
0.125--------
则放出热量为0.125Z
两式相加,得到
2CO2+2NaOH=2NaHCO3,由题意知
X=0.375y+0.125Z=0.125(y+Z)+0.25y。
设2CO2+2NaOH=2NaHCO3的反应热为2A。
得2A=y+Z
那么CO2+NaOH=NaHCO3的反应热A=4x-y。
所以答案选C。
先算出CO2和NaOH的物质的量,分别是0.5mol和0.75mol.由题意知,CO2过量。首先发生CO2 + 2NaOH="Na2CO3+H2O"
0.375---0.75--
放出热量为0.375y
然后
CO2 + H2O+Na2CO3=2NaHCO3,设反应热为Z
0.125--------
则放出热量为0.125Z
两式相加,得到
2CO2+2NaOH=2NaHCO3,由题意知
X=0.375y+0.125Z=0.125(y+Z)+0.25y。
设2CO2+2NaOH=2NaHCO3的反应热为2A。
得2A=y+Z
那么CO2+NaOH=NaHCO3的反应热A=4x-y。
所以答案选C。

练习册系列答案
相关题目
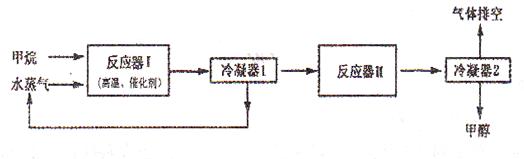
 _____________。
_____________。