题目内容
1.关于物质的量浓度的说法中正确的是( )| A. | 从1L2mol•L-1的NH4Cl溶液中,取出其中的500ml,则其物质的量浓度为1mol•L-1 | |
| B. | 1mol•L-1的NaCl溶液意义就是每升NaCl溶液中含有1molNaCl | |
| C. | 将4gNaOH溶解在100ml水中,所形成的溶液的物质的量浓度1mol•L-1 | |
| D. | 把50m2mol•L-1的CaCl2溶液加水稀释成100ml,则稀释后的溶液中所含的CaCl2的物质的量变成原来的一半 |
分析 A.溶液为均一稳定的分散系;
B.根据物质的量浓度的定义判断;
C.水的体积不等于溶液的体积;
D.稀释前后,浓度发生改变,但溶质的总物质的量不变.
解答 解:A.溶液为均一稳定的分散系,从1L2mol•L-1的NH4Cl溶液中,取出其中的500ml,则其物质的量浓度为2mol•L-1,故A错误;
B.根据物质的量浓度的定义可知1mol•L-1的NaCl溶液意义就是每升NaCl溶液中含有1molNaCl,故B正确;
C.水的体积不等于溶液的体积,将4gNaOH溶解在100ml水中,所形成的溶液的物质的量浓度小于1mol•L-1,故C错误;
D.稀释前后,浓度发生改变,但溶质的总物质的量不变,故D错误.
故选B.
点评 本题考查物质的量浓度的计算,为高频考点,侧重于学生的分析、计算能力的考查,注意把握物质的量浓度的概念,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.下列各组物质在溶液中起反应时,离子方程式相同的是( )
| A. | 氯化钡与硫酸钠,氢氧化钡与硫酸 | |
| B. | 碘化钾与氯气,溴化钾与氯气 | |
| C. | 碳酸银与盐酸,硝酸银与盐酸 | |
| D. | 碳酸氢钠与稀硫酸,碳酸氢钾与盐酸 |
9.下列关于仪器的识别中错误的是( )
| A. | 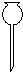 分液漏斗 | B. |  蒸发皿 | C. |  坩埚钳 | D. | 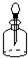 滴瓶 |
16.关于分类的知识说法错误的是( )
| A. | 分类法是学习和研究化学物质及化学变化的一种科学方法 | |
| B. | 常见的分类方法有交叉分类法和树形分类法 | |
| C. | 对于相同的分类对象,采用的分类标准不同,分类的结果也不同 | |
| D. | 初中的化学知识告诉我们,化学反应可以分为化合反应和分解反应两大类 |
13.向含有1molKAl(SO4)2的溶液中逐滴加入氢氧化钡溶液,充分反应.下列说法不正确的是( )
| A. | 当Al3+恰好完全沉淀时,消耗氢氧化钡1.5mol | |
| B. | 当SO42-恰好完全沉淀时,Al3+全部转化为Al(OH)3 | |
| C. | 当向溶液中加入1.5mol氢氧化钡时,反应可用下列离子方程式表示:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ | |
| D. | 反应过程中随加入的氢氧化钡的物质的量不断增大,沉淀的质量不断增大 |
14.已知反应2CH3OH(g)?CH3OCH3(g)+H2O(g)某温度下的平衡常数为400.此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
下列叙述中正确的是( )
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度(mol•L-1) | 0.44 | 0.6 | 0.6 |
| A. | 该反应的平衡常数表达式为:K=[c(CH3OCH3)×c(H2O)]/c(CH3OH) | |
| B. | 此时正、逆反应速率的大小:v正<v逆 | |
| C. | 若加入CH3OH后,经10 min达到平衡,此时c(CH3OH)=0.04 mol/L | |
| D. | 10 min达到平衡时,反应速率v(CH3OH)=1.6 mol/(L•min) |

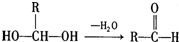
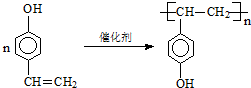 .
.