题目内容
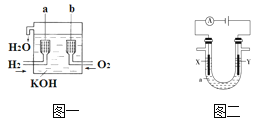
【题目】氢氧燃料电池是一种新型的化学电源,其构造如图一所示:a、b两个电极均由多孔碳制成,通入的气体由孔隙中逸出,并在电极表面放电。
(1)a电极反应式是_______________________;
(2)该燃料电池生成了360 kg的水,则电路中通过了_____________mol的电子。
(3)用如图二所示电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极反应式是___________________。
②Y电极的材料是______________。
【答案】2H2+4OH--4e-=4H2O4×104Cu2++2e-=Cu粗铜
【解析】
(1)氢氧燃料电池中,通入氢气的一极为电源的负极,通入氧气的一极为原电池的正极,因此a电极是负极,因为电解质溶液呈碱性,则负极电极反应式为H2-2e+2OH-=2H2O;
(2)氢氧燃料电池的总反应与氢气在氧气中燃烧的化学方程式相同,生成物为水:2H2+O2=2H2O,当转移电子4mol时,会有2mol即36g的水生成。该燃料电池生成了360 kg的水,即2×104mol的水时会转移电子4×104mol。
(3)①电解方法精炼粗铜,电解池的阴极X材料是纯铜,电极反应为Cu2++2e-=Cu。
②电解方法精炼粗铜,电解池的阳极材料是粗铜,Y电极与电源的正极相连,作阳极,所以Y电极材料是粗铜。

练习册系列答案
相关题目