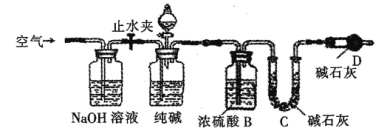
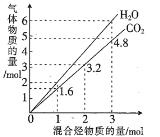
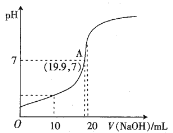
题目内容
【题目】用等体积的0.1mol/L的AgNO3溶液,可使相同物质的量浓度的NaCl、MgCl2和AlCl33种溶液中的Cl-恰好完全沉淀,则3种氯化物溶液的体积之比为( )
A.1:2:3B.3:2:1C.6:3:2D.1:1:1
【答案】C
【解析】
消耗AgNO3的物质的量相等,则NaCl、MgCl2和AlCl3三种溶液中的Cl-物质的量相等,假设为1mol,根据氯离子守恒计算NaCl、MgCl2和AlCl3的物质的量,溶液体积相等,浓度之比等于物质的量之比。
由题意可知,消耗AgNO3的物质的量相等,则NaCl、MgCl2和AlCl3三种溶液中的Cl-物质的量相等,假设为1mol,由氯离子守恒,则:n(NaCl)=1mol、n(MgCl2)=0.5mol、n(AlCl3)=![]() mol,溶液体积相等,浓度之比等于物质的量之比,则c(NaCl):c(MgCl2):c(AlCl3)= 1mol:0.5mol:
mol,溶液体积相等,浓度之比等于物质的量之比,则c(NaCl):c(MgCl2):c(AlCl3)= 1mol:0.5mol:![]() mol=6:3:2,故答案为C。
mol=6:3:2,故答案为C。

 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案【题目】实验室用密度为1.25 gmL﹣1、质量分数为36.5%的浓盐酸配制240 mL 0.1 molL﹣1的盐酸,请回答下列问题:
(1)浓盐酸的物质的量浓度为________________________。
(2)配制240 mL 0.1 molL﹣1的盐酸
应量取浓盐酸体积/mL | 应选用容量瓶的规格/mL |
__________ | __________ |
(3)配制时,其正确的操作顺序是(用字母表示,每个字母只能用一次)__________。
A.用30 mL水洗涤烧杯内壁和玻璃棒23次,洗涤液均注入容量瓶,振荡
B.用量筒淮确量取所需的浓盐酸的体积,倒入烧杯中,再加入少量水(约30 mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线12 cm处
(4)若实验中遇到下列情况,对配制盐酸的物质的量浓度有何影响(填“偏高”“偏低”或“不变”)
①用于稀释盐酸的烧杯未洗涤__________________________________________;
②容量瓶中原有少量蒸馏水____________________________________________;
③定容时俯视观察液面________________________________________________。
(5)若实验过程中出现如下情况如何处理?
①定容时加蒸馏水时超过了刻度________________________________________;
②向容量瓶中转移溶液时不慎有溶液溅出________________________________;
③定容摇匀后发现液面下降____________________________________________。