题目内容
【题目】为探索工业含铝、铁、铜合金废料的再利用,甲同学设计的实验方案如图: 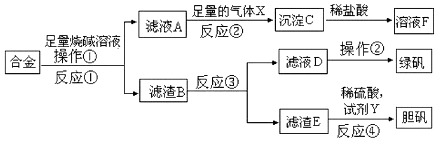
回答下列问题:
(1)操作①的名称为 , 沉淀C的化学式为 .
(2)在滤渣B中滴加稀硫酸时,发现反应速率比同浓度硫酸与纯铁粉反应要快,原因是 .
(3)在滤渣B中滴加的硫酸可用SO2制取,可按以下三步进行: 已知25℃、101kPa时:
2SO2(g)+O2(g)2SO3(g)△H1=﹣197KJ/mol
H2O(g)═H2O(l)△H2=﹣44KJ/mol
2SO2(g)+O2(g)+2H2O(g)═2H2SO4(l)△H3=﹣545KJ/mol
则SO3(g)与H2O(l)反应的热化学方程式是 .
(4)设计实验方案,检测滤液D中含有的金属离子(试剂自选) .
(5)常温下,乙同学将绿矾配成约0.1molL﹣1FeSO4溶液,测得溶液的pH=3,请用离子方程式解释其原因 , 该溶液中c(SO42﹣)﹣c(Fe2+)=molL﹣1(填近似数值).
(6)在滤渣E中加入稀硫酸和试剂Y制胆矾晶体是一种绿色化学工艺,试剂Y为无色液体,则反应④的总反应化学方程式为 .
【答案】
(1)过滤;Al(OH)3
(2)形成铁铜原电池,加快了反应速率
(3)SO3(g)+H2O(l)=H2SO4(l)△H=﹣130kJ/mol
(4)取少量滤液D加入NaOH溶液,产生白色沉淀,沉淀迅速变成灰绿色最后变成红褐色,证明D中有Fe2+或取少量滤液D加入硫氰化钾溶液,无现象,再加入氯水,显血红色,则证明D中有Fe2+
(5)Fe2++2H2O?Fe(OH)2+2H+;5×10﹣4
(6)Cu+H2O2+H2SO4+3H2O═CuSO4?5H2O或Cu+H2O2+H2SO4═CuSO4+2H2O
【解析】解:(1)依据题给信息得出操作①后得到的是滤液和滤渣,故此分离操作为过滤,具体过程为合金加入足量的烧碱溶液后,金属铝可以和强碱氢氧化钠发生反应生成偏铝酸钠和氢气,即2Al+2NaOH+2H2O=2NaAlO2+3H2↑,金属铝溶解,过滤得滤渣B为铁、铜,滤液A中含偏铝酸钠,偏铝酸钠中通入二氧化碳,则可以和二氧化碳气体反应生成氢氧化铝沉淀,即2H2O+AlO2﹣+CO2═Al(OH)3↓+HCO3﹣ , 所以通入足量的气体X为二氧化碳气体,得到沉淀C为氢氧化铝沉淀,所以答案是:过滤;Al(OH)3;(2)在滤渣B中有Cu和Fe,在溶液中形成原电池,铁做负极,铜做正极,形成原电池能加快反应速率,故在滤渣B中滴加稀硫酸时,发现反应速率比一般的铁粉反应要快,所以答案是:形成铜铁原电池,加快了反应速率;(3)2SO2(g)+O2(g)=2SO3(g)△H1=一197kJ/mol ①2H2O (g)=2H2O(1)△H2=﹣44kJ/mol ②2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l)△H3=-545kJ/mol③利用盖斯定律:(③﹣①+②)× ![]() 得SO3 (g)+H2O(l)=H2SO4(l)△H=﹣130kJ/mol,所以答案是:SO3(g)+H2O(l)=H2SO4(l)△H=﹣130kJ/mol;(4)亚铁离子可以和强碱反应生成氢氧化亚铁沉淀,迅速被氧化为氢氧化铁,或用氯水先氧化,再用硫氰化钾溶液检验,故亚铁离子的检验方法:取少量滤液D加入NaOH溶液,产生白色沉淀,沉淀迅速变成灰绿色,最后变成红褐色,或取少量滤液D加入硫氰化钾溶液,无现象,再加入氯水,显血红色,则证明D中有Fe2+;所以答案是:取少量滤液D加入NaOH溶液,产生白色沉淀,沉淀迅速变成灰绿色最后变成红褐色,证明D中有Fe2+或取少量滤液D加入硫氰化钾溶液,无现象,再加入氯水,显血红色,则证明D中有Fe2+;(5)FeSO4溶液中,亚铁离子水解使溶液呈酸性,反应的离子方程式为Fe2++2H2OFe(OH)2+2H+ , 根据电荷守恒有2c(SO42﹣)﹣2c(Fe2+)=c(H+)﹣c(OH﹣)=1×10﹣3 , 所以(SO42﹣)﹣c(Fe2+)=5×10﹣4 , 所以答案是:Fe2++2H2OFe(OH)2+2H+;5×10﹣4;(6)稀硫酸不能将铜氧化,故在滤渣E中加入稀硫酸和H2O2制胆矾晶体,是H2O2将Cu氧化为Cu2+ , H2O2被还原为H2O,稀硫酸只做酸,方程式为:Cu+H2O2+H2SO4+3H2O═CuSO45H2O或Cu+H2O2+H2SO4═CuSO4+2H2O, 所以答案是:Cu+H2O2+H2SO4+3H2O═CuSO45H2O或Cu+H2O2+H2SO4═CuSO4+2H2O.
得SO3 (g)+H2O(l)=H2SO4(l)△H=﹣130kJ/mol,所以答案是:SO3(g)+H2O(l)=H2SO4(l)△H=﹣130kJ/mol;(4)亚铁离子可以和强碱反应生成氢氧化亚铁沉淀,迅速被氧化为氢氧化铁,或用氯水先氧化,再用硫氰化钾溶液检验,故亚铁离子的检验方法:取少量滤液D加入NaOH溶液,产生白色沉淀,沉淀迅速变成灰绿色,最后变成红褐色,或取少量滤液D加入硫氰化钾溶液,无现象,再加入氯水,显血红色,则证明D中有Fe2+;所以答案是:取少量滤液D加入NaOH溶液,产生白色沉淀,沉淀迅速变成灰绿色最后变成红褐色,证明D中有Fe2+或取少量滤液D加入硫氰化钾溶液,无现象,再加入氯水,显血红色,则证明D中有Fe2+;(5)FeSO4溶液中,亚铁离子水解使溶液呈酸性,反应的离子方程式为Fe2++2H2OFe(OH)2+2H+ , 根据电荷守恒有2c(SO42﹣)﹣2c(Fe2+)=c(H+)﹣c(OH﹣)=1×10﹣3 , 所以(SO42﹣)﹣c(Fe2+)=5×10﹣4 , 所以答案是:Fe2++2H2OFe(OH)2+2H+;5×10﹣4;(6)稀硫酸不能将铜氧化,故在滤渣E中加入稀硫酸和H2O2制胆矾晶体,是H2O2将Cu氧化为Cu2+ , H2O2被还原为H2O,稀硫酸只做酸,方程式为:Cu+H2O2+H2SO4+3H2O═CuSO45H2O或Cu+H2O2+H2SO4═CuSO4+2H2O, 所以答案是:Cu+H2O2+H2SO4+3H2O═CuSO45H2O或Cu+H2O2+H2SO4═CuSO4+2H2O.

【题目】人们常用催化剂来选择反应进行的方向.如图所示为一定条件下1mol CH3OH与O2发生反应时,生成CO、CO2或HCHO的能量变化图[反应物O2(g)和生成物H2O(g)略去].
(1)①在有催化剂作用下,CH3OH与O2反应主要生成(填“CO、CO2”或“HCHO”).2HCHO(g)+O2(g)═2CO(g)+2H2O(g)△H= .
②甲醇制取甲醛可用Ag作催化剂,含有AgCl会影响Ag催化剂的活性.用氨水可以溶解除去其中的AgCl,写出该反应的离子方程式: .
(2)已知:CO(g)+2H2(g)CH3OH(g)△H=﹣a kJmol﹣1 .
①经测定不同温度下该反应的平衡常数如下:
温度(℃) | 250 | 300 | 350 |
K | 2.041 | 0.270 | 0.012 |
若某时刻、250℃测得该反应的反应物与生成物的浓度为c(CO)=0.4molL﹣1、c(H2)=0.4molL﹣1、c(CH3OH)=0.8molL﹣1 , 则此时v正v逆(填“>”、“<”或“=”).
②某温度下,在体积固定的2L的密闭容器中将1mol CO和2mol H2混合,测得不同时刻的反应前后压强关系如下:
时间(min) | 5 | 10 | 15 | 20 | 25 | 30 |
压强比(P后/P前) | 0.98 | 0.90 | 0.80 | 0.70 | 0.70 | 0.70 |
则0~15min,用H2表示的平均反应速率为 , 达到平衡时CO的转化率为 .
(3)利用钠碱循环法可除去SO2 , 消除SO2对环境的污染.吸收液吸收SO2的过程中,pH随n(SO32﹣):n(HSO3﹣)变化关系如下表:
n(SO32﹣):n(HSO3﹣) | 91:9 | 1:1 | 1:91 |
pH | 8.2 | 7.2 | 6.2 |
①根据上表判断NaHSO3溶液显性.
②在NaHSO3溶液中离子浓度关系正确的是 (填字母).
a.c(Na+)=2c(SO32﹣)+c(HSO3﹣)
b.c(Na+)>c(HSO3﹣)>c(H+)>c(SO32﹣)>c(OH﹣)
c.c(H2SO3)+c(H+)=c(SO32﹣)+(OH﹣)
d.c(Na+)+c(H+)=c(SO32﹣)+c(HSO3﹣)+c(OH﹣)
【题目】工业上用某矿渣(含有Cu2O(主要)、Al2O3、Fe2O3、SiO2)提取铜的操作流程如图: 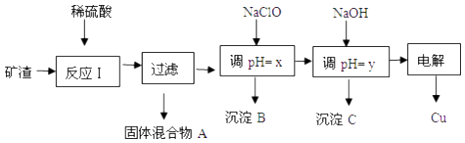
已知:Cu2O+2H+═Cu+Cu2++H2O
沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
开始沉淀pH | 5.4 | 4.0 | 1.1 | 5.8 |
沉淀完全pH | 6.7 | 5.2 | 3.2 | 8.8 |
(1)固体混合物A中的成分是 .
(2)反应Ⅰ完成后,铁元素的存在形式为 . (填离子符号)请写出生成该离子的离子方程式 .
(3)沉淀B可用于制造铁红,为了保证铁红的质量则x的取值为 .
(4)书写出由沉淀C制备铝的化学方程式: .