题目内容
【题目】工业上用某矿渣(含有Cu2O(主要)、Al2O3、Fe2O3、SiO2)提取铜的操作流程如图: 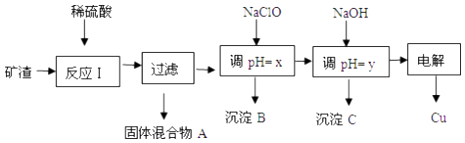
已知:Cu2O+2H+═Cu+Cu2++H2O
沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
开始沉淀pH | 5.4 | 4.0 | 1.1 | 5.8 |
沉淀完全pH | 6.7 | 5.2 | 3.2 | 8.8 |
(1)固体混合物A中的成分是 .
(2)反应Ⅰ完成后,铁元素的存在形式为 . (填离子符号)请写出生成该离子的离子方程式 .
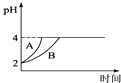
(3)沉淀B可用于制造铁红,为了保证铁红的质量则x的取值为 .
(4)书写出由沉淀C制备铝的化学方程式: .
【答案】
(1)SiO2和Cu
(2)Fe2+2;Fe3++Cu=2Fe2++Cu2+
(3)3.2≤X<4.0
(4)2Al(OH)3 ![]() Al2O3+3H2O、2Al2O3
Al2O3+3H2O、2Al2O3 ![]() 4Al+3O2↑
4Al+3O2↑
【解析】解:(1)Cu2O与酸反应生成Cu和Cu2+ , SiO2与盐酸不反应,固体混合物A为SiO2和Cu;所以答案是:SiO2和Cu;(2)Cu2O与酸反应生成Cu和Cu2+ , Fe2O3与盐酸反应生成Fe3+ , 与Cu反应生成Fe2+:2Fe3++Cu=2Fe2++Cu2+ , 滤液中铁元素为Fe2+;所以答案是:Fe2+;2Fe3++Cu=2Fe2++Cu2+;(3)沉淀B为Fe(OH)3 , 调节pH沉淀铁离子,不沉淀其他离子,根据表中数据可知3.2≤X<4.0可满足;所以答案是:3.2≤X<4.0;(4)沉淀C为Al(OH)3 , 灼烧得到氧化铝,电解熔融态的氧化铝可得铝,涉及的反应为:2Al(OH)3 ![]() Al2O3+3H2O;2Al2O3
Al2O3+3H2O;2Al2O3 ![]() 4Al+3O2↑;所以答案是:2Al(OH)3
4Al+3O2↑;所以答案是:2Al(OH)3 ![]() Al2O3+3H2O、2Al2O3
Al2O3+3H2O、2Al2O3 ![]() 4Al+3O2↑.
4Al+3O2↑.

练习册系列答案
相关题目