题目内容
【题目】如图,△H1=﹣393.5kJmol﹣1 , △H2=﹣395.4kJmol﹣1 , 下列说法正确的是( ) 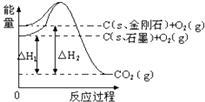
A.金刚石的稳定性强于石墨
B.12g石墨总键能比12g金刚石小1.9kJ
C.石墨和金刚石的转化是物理变化
D.C(s、石墨)=C(s、金刚石)△H=+1.9 kJ/mol
【答案】D
【解析】解:由图得:①C(S,石墨)+O2(g)=CO2(g)△H=﹣393.5kJmol﹣1②C(S,金刚石)+O2(g)=CO2(g)△H=﹣395.4kJmol﹣1 ,
利用盖斯定律将①﹣②可得:C(S,石墨)=C(S,金刚石)△H=+1.9kJmol﹣1 , 则
A、由图象可知,金刚石能量大于石墨的总能量,物质的量能量越大越不稳定,则石墨比金刚石稳定,故A错误;
B、依据热化学方程式 C(S,石墨)=C(S,金刚石)△H=+1.9kJmol﹣1 , 12g石墨的总键能比1 mol金刚石的总键能大于1.9 kJ,故B错误;
C、石墨转化为金刚石是发生的化学反应,属于化学变化,故C错误;
D、因C(s、石墨)=C(s、金刚石)△H=+1.9kJmol﹣1 , 故D正确;
故选D.
【考点精析】利用反应热和焓变对题目进行判断即可得到答案,需要熟知在化学反应中放出或吸收的热量,通常叫反应热.

练习册系列答案
相关题目