��Ŀ����
����Ŀ���Ȼ�隣������̿��Ʊ��ߴ���̼���̵Ĺ�����������
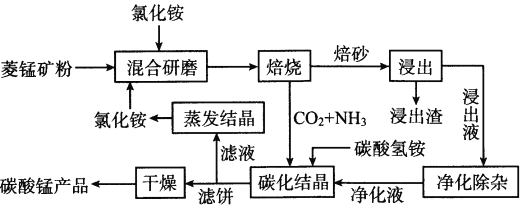
��֪�������̿����Ҫ�ɷ���MnCO3����������Fe��Al��Ca��Mg��Ԫ�ء�
����ؽ�������[c0(Mn+)=0.1mol/L�γ��������������pH��Χ���£�

�۳����£�CaF2��MgF2���ܶȻ��ֱ�Ϊ1.46��10��10��7.42��10��11��
�ش��������⣺
��1����������ʱ��������Ҫ��Ӧ�Ļ�ѧ����ʽΪ__________________��
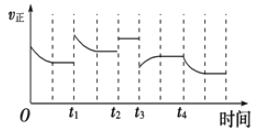
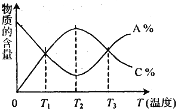
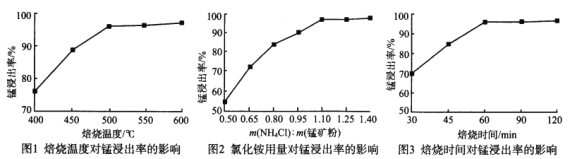
��������ͼ1��ͼ2��ͼ3���Ȼ�隣������̿����������ǣ������¶�Ϊ_________���Ȼ�����̿�۵�����֮��Ϊ_________������ʱ��Ϊ_________��
��2������Һ�������������������£����ȼ���MnO2��Fe2+����ΪFe3+����Ӧ�����ӷ���ʽΪ_________���ٵ�����Һ��pH��Al3+��Fe3+��Ϊ������ȥ����ҺpH�ķ�ΧΪ_________��Ȼ�����NH4F��Ca2+��Mg2+��ΪCaF2��MgF2������ȥ�����ֳ�������ʱ��Һ��c(Ca2+)/c(Mg2+)=_________��
��3��̼���ᾧʱ����Ӧ�����ӷ���ʽΪ__________________��
��4�����Ƶõĸߴ���̼�������ڹ���ϡ������ö��Ե缫��⣬��ij���õ���Ҫ�������ܲ���MnO2���õ缫�ĵ缫��ӦʽΪ__________________��
���𰸡�MnCO3��2NH4Cl![]() MnCl2��2NH3����CO2����H2O 500�� 1.10 60min MnO2��2Fe2����4H��=Mn2����2Fe3����2H2O 5.2��pH<8.8 1.97 Mn2����2HCO3��
MnCl2��2NH3����CO2����H2O 500�� 1.10 60min MnO2��2Fe2����4H��=Mn2����2Fe3����2H2O 5.2��pH<8.8 1.97 Mn2����2HCO3��![]() MnCO3��CO2����H2O Mn2����2H2O��2e��=MnO2��4H��
MnCO3��CO2����H2O Mn2����2H2O��2e��=MnO2��4H��
��������
��1��NH4Cl�ֽ�ΪNH3��HCl��HCl��MnCO3��Ӧ�õ�MnCl2��CO2��H2O���ɴ�д������ʽ��
��ͼ1��ͼ2��ͼ3���̽�����ѡ�����������
��2��MnO2�����������½�Fe2������ΪFe3����
��ʹAl3+��Fe3+��Ϊ������ȥ����ҺpH��5.2����ʹMn2+������pH<8.8���Ӷ�ȷ��pH��Χ��
��ƽ�ⳣ���������ֳ�������ʱ��Һ��![]() ��
��
��3��̼���ᾧʱ���ɿ���Mn��HCO3��2���ȷֽ⣬���д�����ӷ��̡�
��4�������õ���Ҫ�������ܲ���MnO2��ʧ���ӷ���������Ӧ��
��1��NH4Cl�ֽ�ΪNH3��HCl��HCl��MnCO3��Ӧ�õ�MnCl2��CO2��H2O����Ӧ����ʽΪMnCO3��2NH4Cl![]() MnCl2��2NH3����CO2����H2O��
MnCl2��2NH3����CO2����H2O��
�Ȼ�隣������̿����������ǣ������¶�Ϊ500�����Ȼ�����̿�۵�����֮��Ϊ1.10������ʱ��Ϊ60min��
��2��MnO2�����������½�Fe2������ΪFe3�������ӷ���ʽΪ��MnO2��2Fe2����4H��=Mn2����2Fe3����2H2O��
��ʹAl3+��Fe3+��Ϊ������ȥ����ҺpH��5.2����ʹMn2+������pH<8.8,��ҺpH�ķ�ΧΪ5.2��pH<8.8��
����NH4F��Ca2+��Mg2+��ΪCaF2��MgF2������ȥ�����ֳ�������ʱ��Һ��![]() =1.46��10��10/7.42��10��11=1.97.
=1.46��10��10/7.42��10��11=1.97.
��3���ɿ���Mn��HCO3��2���ȷֽ⣬���ӷ���ʽΪ��Mn2����2HCO3��![]() MnCO3��CO2����H2O��
MnCO3��CO2����H2O��
��4�� ���Ƶõĸߴ���̼�������ڹ���ϡ������ö��Ե缫��⣬�������õ���Ҫ�������ܲ���MnO2���õ缫�ĵ缫��ӦʽΪMn2����2H2O��2e��=MnO2��4H����������ӦΪ��2H����2e��=H2����