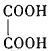��Ŀ����
����Ŀ��һ�������£������Ϊ3L���ܱ������У�һ����̼��������Ӧ���ɼ״�(����ΪCu2O/ZnO)��CO(g)��2H2(g)![]() CH3OH(g)��������������������⣺
CH3OH(g)��������������������⣺
(1)��Ӧ�ﵽƽ��ʱ��ƽ�ⳣ������ʽK��__________�������¶ȣ�Kֵ________(��������������С������������)��ƽ����__________�����ƶ���
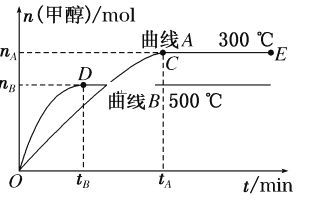
(2)��500 �����ӷ�Ӧ��ʼ��ƽ�⣬������ƽ����Ӧ����v(H2)____________________�����ú���Ӧ��ĸ��ʽ�ӱ�ʾ��
(3)�������������������£�������E�����ϵ���ѹ����ԭ����1/2�������йظ���ϵ��˵����ȷ����________(��ѡ����ĸ)��
A��������Ũ�ȼ�С B������Ӧ���ʼӿ죬�淴Ӧ����Ҳ�ӿ�
C���״������ʵ������� D������ƽ��ʱ![]() ����
����
(4)���о�����Ӧ������������õ�ΪCu2O����Ӧ��ϵ�к�����CO2������ά�ִ���Cu2O�������䣬ԭ����_________________________________(�û�ѧ����ʽ��ʾ)��
���𰸡�![]() ��С �淴Ӧ
��С �淴Ӧ ![]() BC Cu2O��CO
BC Cu2O��CO![]() 2Cu��CO2
2Cu��CO2
��������
��1����֪CO(g)+2H2(g)CH3OH(g)����K=![]() ��500��ʱ�״������ʵ���С�����������¶ȣ�ƽ�����ƣ�����K��С���ʴ�Ϊ��
��500��ʱ�״������ʵ���С�����������¶ȣ�ƽ�����ƣ�����K��С���ʴ�Ϊ��![]() ����С���淴Ӧ��
����С���淴Ӧ��
��2����500�棬ƽ��ʱͼ�м״��ı仯��ΪnB�����Է�Ӧ���ĵ���������Ϊ��2nB����![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
��3���������������������£��Դ���E�����ϵ���ѹ����ԭ����1/2����ѹǿ�������淴Ӧ���ʶ�����ƽ���������ƶ����״������ʵ������࣬���������ʵ�����С�������������С��ƽ��ʱ������Ũ�ȷ���������Ũ�ȱ�ֵ�������ʵ�����ֵ����������ƽ��ʱ![]() ��С����BC��ȷ���ʴ�Ϊ��BC��
��С����BC��ȷ���ʴ�Ϊ��BC��
��4����Ӧ��ϵ�к�����CO2������ά�ִ���Cu2O�������䣬һ����̼��������ͭ��Ӧ����ͭ�Ͷ�����̼����Ӧ�Ļ�ѧ����ʽ��Cu2O+CO2Cu+CO2��������̼���Ʒ�Ӧ������У�������ά�ִ���Cu2O�������䣬�ʴ�Ϊ��Cu2O+CO2Cu+CO2��

 ������ʱͬ����ϰ��ϵ�д�
������ʱͬ����ϰ��ϵ�д� ѧҵ����һ��һ��ϵ�д�
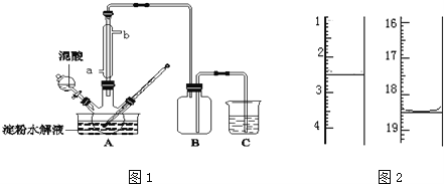
ѧҵ����һ��һ��ϵ�д�����Ŀ������ʵ��װ��������Ӧ������ȷ����(����)
ѡ�� | A | B | C | D |
װ�� |
|
|
|
|
���� | ��֤��Al(OH)3�����ڰ�ˮ | ��֤���ǽ����ԣ�Cl>C>Si | ��֤���������ⸯʴ | ϴ��ƿ�в����İ�ɫ������BaSO3 |
A. A B. B C. C D. D
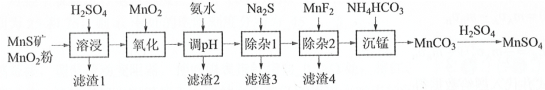
����Ŀ���ߴ���������Ϊ�ϳ���������Ԫ�������ϵ�ԭ�ϣ���ҵ�Ͽ�����Ȼ�������̷������̿���Fe��Al��Mg��Zn��Ni��Si��Ԫ��������Ʊ�����������ͼ��ʾ���ش��������⣺
��ؽ�������[c0(Mn+)=0.1 molL1]�γ��������������pH��Χ���£�
�������� | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Zn2+ | Ni2+ |
��ʼ������pH | 8��1 | 6��3 | 1��5 | 3��4 | 8��9 | 6��2 | 6��9 |
������ȫ��pH | 10��1 | 8��3 | 2��8 | 4��7 | 10��9 | 8��2 | 8��9 |
(1)������1������S��__________________________��д�����ܽ����ж������������̷�Ӧ�Ļ�ѧ����ʽ____________________________________________________��
(2)��������������������MnO2�������ǽ�________________________��
(3)����pH��������������Һ��pH��ΧӦ����Ϊ_______~6֮�䡣
(4)д�������̡������ӷ���ʽ_____________��
(5)��״��������Ԫ���Ͽ���Ϊ����ӵ���������ϣ��仯ѧʽΪLiNixCoyMnzO2������Ni��Co��Mn�Ļ��ϼ۷ֱ�Ϊ+2��+3��+4����x=y=![]() ʱ��z=__________��
ʱ��z=__________��