题目内容
5.下列关于反应KClO3+6HCl(浓)═KCl+3Cl2↑+3H2O说法正确的是( )| A. | 还原剂是KClO3 | B. | HCl被还原 | ||
| C. | 得到3molCl2转移6mol电子 | D. | 氧化产物、还原产物都是Cl2 |
分析 KClO3+6HCl(浓)═KCl+3Cl2↑+3H2O中,Cl元素的化合价由+5价降低为0,Cl元素的化合价由-1价升高为0,以此来解答.
解答 解:A.Cl元素的化合价由+5价降低为0,则KClO3为氧化剂,故A错误;
B.Cl元素的化合价由-1价升高为0,则Cl为还原剂,故B错误;
C.由反应可知,得到3molCl2转移5mol电子,故C错误;
D.只有Cl元素的化合价变化,则氧化产物、还原产物都是Cl2,故D正确;
故选D.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意HCl的作用及氧化还原反应基本概念,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
13.下列说法不正确的是( )
| A. | 金刚石、石英和足球烯均为空间网状结构的原子晶体 | |
| B. | 在NaOH、NH4Cl和Na2S04中,都存在离子键和共价键 | |
| C. | 干冰升华的过程只需克服分子间作用力 | |
| D. | H20分解生成H2和O2的过程中既有共价键断裂,又有共价键形成 |
20.下列说法正确的是( )
| A. | 按系统命名法,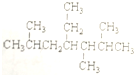 的名称为2,5,6-三甲基-4-乙基庚烷 的名称为2,5,6-三甲基-4-乙基庚烷 | |
| B. | 常压下,正戊烷、异戊烷、新戊烷的沸点依次升高 | |
| C. | 甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应 | |
| D. | 2-甲基-1,3-丁二烯的键线式为 |
10.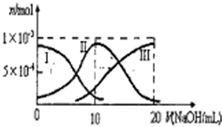 常温下,向10mL0.1mol•L-1H2A溶液中滴加0.1mol•L-1NaOH:溶液.有关微粒的物质的量变化如图(其中I代表、H2A,Ⅱ代表ⅡAⅢ代表A2-).根据图示判断,下列说法不正确的是( )
常温下,向10mL0.1mol•L-1H2A溶液中滴加0.1mol•L-1NaOH:溶液.有关微粒的物质的量变化如图(其中I代表、H2A,Ⅱ代表ⅡAⅢ代表A2-).根据图示判断,下列说法不正确的是( )
 常温下,向10mL0.1mol•L-1H2A溶液中滴加0.1mol•L-1NaOH:溶液.有关微粒的物质的量变化如图(其中I代表、H2A,Ⅱ代表ⅡAⅢ代表A2-).根据图示判断,下列说法不正确的是( )
常温下,向10mL0.1mol•L-1H2A溶液中滴加0.1mol•L-1NaOH:溶液.有关微粒的物质的量变化如图(其中I代表、H2A,Ⅱ代表ⅡAⅢ代表A2-).根据图示判断,下列说法不正确的是( )| A. | 当V(NaOH)=10mL时,溶液中离子浓度的关系一有定:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) | |
| B. | 当V(NaOH)=15mL时,溶液中离子浓度的关系一定有:c(HA-)+2c(H+)+3c(H2A)=c(A2-)+2c(OH-) | |
| C. | 当V(NaOH)=15mL时,向溶液中滴加少量的盐酸或NaOH溶液,溶液的pH保持不变 | |
| D. | 当V(NaOH)=20mL时,向溶液中加水稀释,c(H+)减小,Kw不变 |
14.某化学科研小组对周围大气进行监测,发现该地区首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5微米的悬浮颗粒物),其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:
(1)将PM2.5样本用蒸馏水处理制成待测试样,若测得该试样所含水溶性无机离子的化学组分及其平均浓度如表:
根据表中数据判断PM2.5的酸碱性为酸性,试样的pH=4.
(2)①为减少SO2的排放,可洗涤含SO2的烟气,作为洗涤剂下列物质最好选择a(填字母).
a. 氨水 b. Na2CO3 c.O2 d.NaHSO3
②浓度均为0.1mol/L (NH4)2Fe(SO4)2、NH4HSO4、(NH4)2SO3,其中c(NH4+)最大的是(NH4)2Fe(SO4)2(填化学式).
(3)①已知汽缸中生成NO的反应为N2(g)+O2(g)?2NO(g)△H>0,汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是吸热反应,温度升高,平衡正向移动,NO含量增大.
②汽车燃油不完全燃烧时产生CO,有人设计下列反应除去CO:2CO(g)═2C(s)+O2(g),已知该反应的△H>0,简述该设想能否实现的依据①②△H>0△S<0,则在任何温度下△G>0,不可能自发进行.
(1)将PM2.5样本用蒸馏水处理制成待测试样,若测得该试样所含水溶性无机离子的化学组分及其平均浓度如表:
| 离 子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
(2)①为减少SO2的排放,可洗涤含SO2的烟气,作为洗涤剂下列物质最好选择a(填字母).
a. 氨水 b. Na2CO3 c.O2 d.NaHSO3
②浓度均为0.1mol/L (NH4)2Fe(SO4)2、NH4HSO4、(NH4)2SO3,其中c(NH4+)最大的是(NH4)2Fe(SO4)2(填化学式).
(3)①已知汽缸中生成NO的反应为N2(g)+O2(g)?2NO(g)△H>0,汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是吸热反应,温度升高,平衡正向移动,NO含量增大.
②汽车燃油不完全燃烧时产生CO,有人设计下列反应除去CO:2CO(g)═2C(s)+O2(g),已知该反应的△H>0,简述该设想能否实现的依据①②△H>0△S<0,则在任何温度下△G>0,不可能自发进行.
15.为达到预期的实验目的,下列操作正确的是( )
| A. | 向无色溶液中加BaCl2溶液,生成白色沉淀,再加稀硝酸,沉淀不消失,由此确定该溶液中一定含有SO${\;}_{4}^{2-}$ | |
| B. | 用pH试纸测定氯水的pH | |
| C. | 欲制备Fe(OH)3胶体,向盛有沸水的烧杯中滴加FeCl3饱和溶液并长时间煮沸 | |
| D. | 为鉴别KCl、AlCl3和MgCl2溶液,分别向三种溶液中滴加NaOH溶液至过量 |
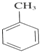 +3HNO3$→_{△}^{浓硫酸}$
+3HNO3$→_{△}^{浓硫酸}$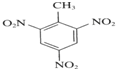 +3H2O,取代反应.
+3H2O,取代反应.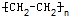 ,加聚反应(或聚合反应).
,加聚反应(或聚合反应).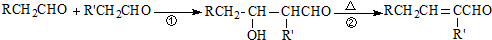
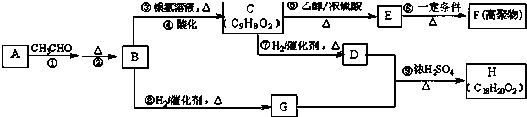
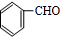 .
.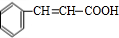 +CH3CH2OH$→_{△}^{浓H_{2}SO_{4}}$
+CH3CH2OH$→_{△}^{浓H_{2}SO_{4}}$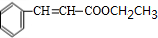 +H2O
+H2O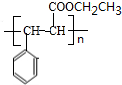
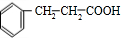 +
+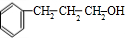 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$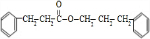 +H2O.
+H2O.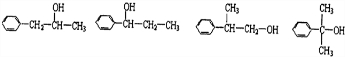 .
.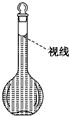 实验室需要配置0.50mol/L NaCl溶液500mL.按下列操作步骤填上适当的文字,以使整个操作完整.
实验室需要配置0.50mol/L NaCl溶液500mL.按下列操作步骤填上适当的文字,以使整个操作完整.