题目内容
15.写出下列反应的化学方程式,并注明反应类型(1)将乙烯通入溴的四氯化碳溶液中CH2=CH2+Br2→CH2Br-CH2Br;加成反应.
(2)甲苯与浓硝酸反应
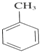 +3HNO3$→_{△}^{浓硫酸}$
+3HNO3$→_{△}^{浓硫酸}$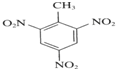 +3H2O,取代反应.
+3H2O,取代反应.(3)甲烷与氯气的第一步反应CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl,取代反应.
(4)乙烯生成聚乙烯nCH2=CH2$→_{△}^{催化剂}$
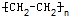 ,加聚反应(或聚合反应).
,加聚反应(或聚合反应).
分析 (1)乙烯含有碳碳双键,可发生加成反应生成1,2-二溴乙烷;
(2)甲苯和浓硝酸在浓硫酸催化作用下加热反应生成三硝基甲苯和水;
(3)甲烷和氯气发生取代反应第一步反应生成一氯甲烷;
(4)乙烯含有碳碳双键,可发生加聚反应生成聚乙烯.
解答 解:(1)乙烯含有碳碳双键,与溴发生加成反应,化学方程式为:CH2=CH2+Br2→CH2Br-CH2Br,属于加成反应;
故答案为:CH2=CH2+Br2→CH2Br-CH2Br,加成反应;
(2)甲苯易发生取代反应,和浓硝酸之间发生取代反应生成2,4,6-三硝基甲苯,即TNT,方程式为 +3HNO3$→_{△}^{浓硫酸}$
+3HNO3$→_{△}^{浓硫酸}$ +3H2O,
+3H2O,
故答案为: +3HNO3$→_{△}^{浓硫酸}$
+3HNO3$→_{△}^{浓硫酸}$ +3H2O,取代反应;
+3H2O,取代反应;
(3)甲烷和氯气发生取代反应第一步反应生成一氯甲烷,方程式为:CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl,
故答案为:CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl,取代反应;
(4)乙烯含有碳碳双键,可发生加聚反应生成聚乙烯,方程式为nCH2=CH2$→_{△}^{催化剂}$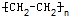 ,
,
故答案为:nCH2=CH2$→_{△}^{催化剂}$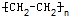 ,加聚反应(或聚合反应).
,加聚反应(或聚合反应).
点评 本题考查有机物的结构和性质以及反应类型,为高考常见题型,注意把握有机物的官能团的性质以及相关方程式的书写,为解答该题的关键,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.能发生加成反应,也能发生取代反应,同时能使溴水因反应而褪色,也能使酸性高锰酸钾溶液褪色的是D;
A. B.
B.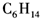 C.
C.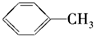 D.
D.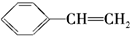
该分子与溴水反应的方程式为 ,该分子也是生产某塑料的单体,写出合成该塑料的化学方程式:
,该分子也是生产某塑料的单体,写出合成该塑料的化学方程式: .
.
A.
 B.
B.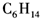 C.
C. D.
D.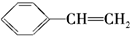
该分子与溴水反应的方程式为
 ,该分子也是生产某塑料的单体,写出合成该塑料的化学方程式:
,该分子也是生产某塑料的单体,写出合成该塑料的化学方程式: .
.
6.28g铜金合金与足量的某浓度HNO3反应,将产生的气体和2.24L(标准状况)O2混合,通入水中,气体恰好被完全吸收,则合金中铜的质量为( )
| A. | 9.6g | B. | 6.4g | C. | 12.8g | D. | 8g |
3.在含0.2molKOH和0.1molBa(OH)2混合溶液中持续通入CO26.72L(标况)的过程中,溶液中离子的物质的量n和通入CO2体积V关系示意图正确的是( )
| A | B | C | D |
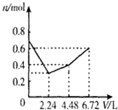 |  | 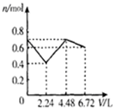 | 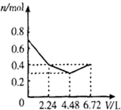 |
| A. | A | B. | B | C. | C | D. | D |
10.有关元素及其化合物知识的说法正确的是( )
| A. | 浓硝酸能与木炭反应,证明浓硝酸既具有强氧化性又具有强酸性 | |
| B. | 浓硫酸具有吸水性,因而能使蔗糖炭化 | |
| C. | 高温下SiO2与Na2CO3反应生成Na2SiO3和CO2,证明硅酸酸性强于碳酸 | |
| D. | 铵盐受热都能分解,但不一定都能生成氨气 |
7.25℃,101kPa时,使1.0g钠与足量氯气反应,生成氯化钠晶体并放出17.87kJ的热量,生成1mo NaCl的反应热为( )
| A. | 17.87kJ | B. | -17.87kJ/mol | C. | 411 kJ/mol | D. | -411 kJ/mol |
4.钴的氧化物广泛应用于磁性材料及超导材料等领域.取一定量的钴的氧化物(其中钴的化合价为+2、+3价),用480mL 5mol•L-1盐酸恰好完全溶解固体,得到CoCl2溶液和4.48L(标准状况)黄绿色气体.通过计算可以确定该氧化物中Co、0的物质的量之比为( )
| A. | 1:1 | B. | 2:3 | C. | 3:4 | D. | 5:6 |
5.下列关于反应KClO3+6HCl(浓)═KCl+3Cl2↑+3H2O说法正确的是( )
| A. | 还原剂是KClO3 | B. | HCl被还原 | ||
| C. | 得到3molCl2转移6mol电子 | D. | 氧化产物、还原产物都是Cl2 |