题目内容
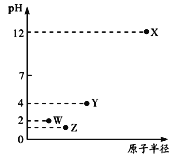
【题目】第三周期元素X、Y、Z、W的最高价氧化物溶于水可得四种溶液,0.01mol/L的这四种溶液pH与该元素原子半径的关系如下图所示。下列说法正确的是
A. 简单离子半径: X>Y>Z>W
B. W的单质在常温下是黄绿色气体
C. 气态氢化物的稳定性: Z>W>Y
D. X和Y的最高价氧化物对应的水化物恰好中和时,溶液中的微粒共有2种
【答案】B
【解析】
第三周期元素中,X最高价氧化物水化物的溶液pH为12,氢氧根浓度为0.01mol/L,故为一元强碱,则X为Na元素;Y、W、Z对应的最高价氧化物水化物的溶液pH均小于7,均为酸,W最高价含氧酸溶液中氢离子浓度为0.01mol/L,故为一元强酸,则W为Cl元素;最高价含氧酸中,Z对应的酸性比W的强、Y对应的酸性比W的弱,而原子半径Y>Z>Cl,SiO2不溶于水,故Z为S元素,Y为P元素,以此解答该题。
综上所述可知X是Na元素,Y是P元素,Z是S元素,W是Cl元素。
A.离子的电子层结构相同,核电荷数越大,离子半径越小;离子的电子层越多,离子半径越大,离子半径P3->S2->Cl->Na+,A错误;
B.W是Cl元素,其单质Cl2在常温下是黄绿色气体,B 正确;
C.元素的非金属性越强,其简单氢化物的稳定性就越强,由于元素的非金属性W>Z>Y,所以气态氢化物的稳定性:W>Z>Y,C错误;
D.X和Y的最高价氧化物对应的水化物分别为NaOH、H3PO4,二者恰好中和时生成磷酸钠,由于该盐是强碱弱酸盐,溶液中磷酸根发生分步水解反应,产生HPO42-,产生的HPO4-会进一步发生水解反应产生H2PO4-、H3PO4,同时溶液中还存在H+、OH-,因此溶液中的微粒种类比2种多,D错误;
故合理选项是B。

练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目