��Ŀ����
����Ŀ��ȼú�������к���SO2��Ϊ�����������������������ö��ַ���ʵ����������
��1����ʪʽ���շ����������ռ���SO2������Ӧ�Ӷ����������Լ����ʺ������÷����ռ�����______������ĸ��ţ���
a��ʯ����b��CaCl2��Һ
��2��ij�������ú�SO2������������Cr2O72-�����Է�ˮ���������з�Ӧ��ĸ�Ԫ����Cr3+��ʽ���ڣ������������£�
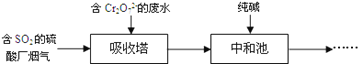
����SO2����������ˮʱ��������SO2��______�ԡ�
���������з�����Ӧ�����ӷ���ʽΪ____________________________________��
��3���÷�ˮ����������й��������£��������Ӻ��Բ��ƣ���
���� | Cr2O72�� | Cr3+ | H + | Na + | SO42�� |
Ũ�ȣ�mol/L�� | a | 0.2��10��6 | 1.2��10��6 | 6.8��10��6 | 3.0��10��6 |
��a�� ______��
���𰸡� a ��ԭ 3SO2+Cr2O72��+2H+��2Cr3++3SO42-+H2O 1.3��10��6
����������1��a����������������������������ʯ���鷴Ӧ��a��ȷ��b�����������ǿ����������CaCl2��Һ���������Ӧ��b��������ѡa����2���ٷ�Ӧ��CrԪ�ػ��ϼ۴�+6�۽��͵�+3�ۣ��õ�3�����ӣ���˶�������ʧȥ���ӣ���������������SO2����������ˮʱ��������SO2�Ļ�ԭ�ԡ��ڶ�����������Ԫ�ػ��ϼ۴�+4�����ߵ�+6�ۣ�ʧȥ2�����ӣ����ݵ��ӵ�ʧ�غ��ԭ���غ��Լ�����غ��֪�������з�����Ӧ�����ӷ���ʽΪ3SO2+Cr2O72��+2H+��2Cr3++3SO42-+H2O����3�����ݵ���غ��֪2��amol/L+2��3.0��10��6mol/L��1.2��10��6 mol/L +6.8��10��6 mol/L +3��0.2��10��6mol/L�����a��1.3��10��6��