题目内容
【题目】A、B、X、Y和Z是原子序数依次递增的短周期元素。其中A与Y同主族,X与Z同主族,A与B和X均可形成10个电子的化合物;B与Z的最外层电子数之比为2∶3,常见化合物Y2X2与水反应生成X的单质,其水溶液可使酚酞试液变红。请回答下列问题:
(1)Z元素在元素周期表中的位置是_____________________。
(2)化合物B2A4的结构式为____________________。
(3)A与X、A与Z均能形成18个电子的化合物,此两种化合物发生反应的化学方程式为_____
(4)将Z与X形成的气态化合物ZX2通入Ba(NO3)2溶液中,有白色沉淀和NO气体生成,发生反应的离子方程式为________________________________________________,由此可得出NO与ZX2的还原性大小关系为________________(填相应化学式)。
(5)将Y2X2投入到Y2Z的水溶液中可生成Z的单质,发生反应的化学方程式为________。
(6)两种均含A、X、Y、Z四种元素的化合物相互反应放出气体的离子反应方程式为________。
【答案】 第三周期第VIA族 ![]() H2O2+H2S=S↓+2H2O 3SO2+3Ba2++2NO3-+2H2O=3BaSO4↓+2NO+4H+ SO2>NO Na2O2+Na2S+2H2O=S+4NaOH HSO3-+H+=SO2↑+H2O
H2O2+H2S=S↓+2H2O 3SO2+3Ba2++2NO3-+2H2O=3BaSO4↓+2NO+4H+ SO2>NO Na2O2+Na2S+2H2O=S+4NaOH HSO3-+H+=SO2↑+H2O
【解析】
A、B、X、Y和Z是原子序数依次递增的短周期元素,常见化合物Y2X2与水反应生成X的单质,其水溶液可使酚酞试液变红,应该是过氧化钠和水反应生成氢氧化钠和氧气,则X为O元素,则Y为Na元素;A与X可形成10个电子化合物,A与Y同主族,则A为H元素;X与Z同主族,则Z为S元素;B与Z的最外层电子数之比为2:3,则B元素的最外层电子数为4,A与B可形成10个电子化合物,B为C元素,据此解答。
根据以上分析可知A是H,B是C,X是O,Y是Na,Z是S。则
(1)S元素在元素周期表中的位置是第三周期第VIA族;
(2)化合物B2A4是乙烯,结构式为![]() ;
;
(3)H与O、H与S均能形成18个电子的化合物,分别是H2O2、H2S,H2O2可将H2S氧化成S,故方程式为H2O2+H2S=S↓+2H2O;
(4)将S与O形成的气态化合物SO2通入Ba(NO3)2溶液中,有白色沉淀和NO气体生成,这是由于在酸性溶液中硝酸根把二氧化硫氧化为硫酸,发生反应的离子方程式为3SO2+3Ba2++2NO3-+2H2O=3BaSO4↓+2NO+4H+;根据还原剂的还原性大于还原产物的还原性可判断还原性SO2>NO;
(5)将Na2O2投入到Na2S的水溶液中可生成S的单质,Na2O2将Na2S氧化成S,反应的化学方程式为Na2O2+Na2S+2H2O=S+4NaOH;
(6)两种均含H、O、Na、S四种元素的化合物为NaHSO3和NaHSO4,相互反应放出气体的离子反应方程式为HSO3-+H+=SO2↑+H2O。

 中考解读考点精练系列答案
中考解读考点精练系列答案【题目】燃煤的烟气中含有SO2,为了治理雾霾天气,工厂采用多种方法实现烟气脱硫。
(1)“湿式吸收法”利用吸收剂与SO2发生反应从而脱硫。下列试剂中适合用作该法吸收剂的是______(填字母序号)。
a.石灰乳b.CaCl2溶液
(2)某工厂利用含SO2的烟气处理含Cr2O72-的酸性废水,吸收塔中反应后的铬元素以Cr3+形式存在,具体流程如下:
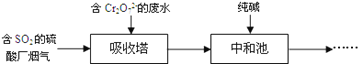
①用SO2处理含铬废水时,利用了SO2的______性。
②吸收塔中发生反应的离子方程式为____________________________________。
(3)该废水经处理后,测得有关数据如下(其他离子忽略不计):
离子 | Cr2O72- | Cr3+ | H + | Na + | SO42- |
浓度(mol/L) | a | 0.2×10-6 | 1.2×10-6 | 6.8×10-6 | 3.0×10-6 |
则a= ______。